题目内容
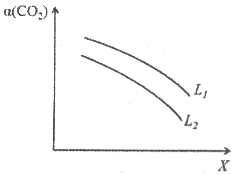
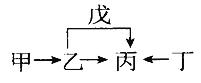
【题目】A、B、C、D、E、F 是原子序数依次增大的短周期主族元素。E 是同周期金属性最强的元素。甲、乙、丙、丁、戊是由上述部分元素中的两种或几种组成的化合物,它们之间的转化关系如图所示。其中甲是生活中的调味品,丁是淡黄色固体。下列说法不正确的是
A. 元素B的氢化物可能具有正四面体结构
B. 元素上的氧化物对应水物化的酸性一定比硫酸的酸性强
C. 原子半径:r(E)>r(F)>r(C)>r(D)
D. 化合物A4BC2D既可能是共价化合物,也可是离子化合物
【答案】B
【解析】A、B、C、D、E、F是原子序数依次增大的短周期主族元素。E是同周期金属性最强的元素,则E为钠元素,其中甲是生活中的调味品,甲为氯化钠,丁是淡黄色固体,丁为过氧化钠。甲、乙、丙、丁、戊是由上述部分元素中的两种或几种组成的化合物,它们之间的转化关系如图所示。假如乙为氢氧化钠,丙为碳酸钠,戊为二氧化碳,则符合流程,故A、B、C、D、E、F分别为H、C、N、O、Na、Cl,A. 元素B的氢化物CH4具有正四面体结构,选项A正确;B. 元素F的氧化物对应水化物有高氯酸、氯酸、次氯酸,次氯酸的酸性比硫酸的酸性弱,选项B不正确;C. 同周期元素从左到右依次减小,同主族元素原子半径从上而下依次增大,故原子半径:r(E)>r(F)>r(C)>r(D),选项C正确;D. 化合物A4BC2D若为CO(NH2)2则是共价化合物,若为NH4CNO则是离子化合物,选项D正确。答案选B。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案【题目】r—Fe2O3是一种具有磁性、催化、气敏的纳米材料。一种以硫铁矿烧渣等为原料制备r—Fe2O3的流程如下:

(1)下列有关“还原焙烧”工序的说法正确的是_____(填字母)。
a.焦炭应少量,空气应过量
b. 焙烧过程均为吸热反应,需用电炉持续加热反应器
c.“还原焙烧”的主要反应为 3C+2O2![]() 2CO+CO2、Fe2O3+CO
2CO+CO2、Fe2O3+CO![]() 2FeO+CO2
2FeO+CO2
(2)“浸取”前需将焙烧生成的熔体粉碎,其目的是_____________________。
(3)已知三种金属离子开始沉淀和完全沉淀的pH如下表:
Fe3+ | Fe2+ | Al3+ | |
开始沉淀的pH | 2.2 | 7.5 | 4.1 |
完全沉淀的pH | 3.5 | 9.5 | 5.4 |
则“调pH”时,溶液的pH范围为_______________。
(4)滤渣1的主要成分为_________(填化学式);“沉铁”时发生反应的离子方程式为___________。
(5)“过滤2”时需用蒸馏水洗涤,能证明沉淀已洗涤干净的方法是_________;沉淀缓慢氧化为铁黄的化学方程式为________________。
【题目】I. 常温下,将3种一元酸分别和NaOH溶液等体积混合,实验数据如下:
组别 | c(一元酸)或c(H+) | c(NaOH)/mol/L | 混合溶液的pH |
甲 | c(H+)=0.1 mol/L的HX酸 | 0.1 | pH=a |
乙 | c(HY)=0.1mol/L | 0.1 | pH=7 |
丙 | c(HZ)=0.1 mol/L | 0.1 | pH=9 |
(1)甲组实验中HX为弱酸,a______7(填“<”,“=”或“>”)。
(2)乙组实验中HY溶液的pH=______。
(3)丙组实验发生反应的离子方程式为__________________,
所得溶液中由水电离出的c(OH-)=______mol/L。
II. 将0.1 mol·L-1 NaOH溶液分别滴入体积均为20 mL、浓度均为0.1 mol·L-1 HCl溶液和HA溶液,溶液的pH随加入NaOH溶液体积变化如图:

(1)HA为_______酸(填“强”或“弱”)。
(2)N点pH>7的原因是(用离子方程式表示)_________。
(3)下列说法正确的是_______ (填字母)。
a. M点c(HA)-)
b. M点c(Na+)>c(OH-)
c. P点c(Cl-)=0.05 mol·L-1
(4)NaA与NaOH等浓度等体积混合时,溶液中c(A-)______c(OH-)(填“<”,“=”或“>”)