题目内容
16.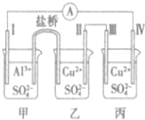 某电化学装置如图所示,电极I为Al,其它均为Cu,且开始时四电极质量均相等,下列叙述正确的是( )
某电化学装置如图所示,电极I为Al,其它均为Cu,且开始时四电极质量均相等,下列叙述正确的是( )| A. | 甲为原电池,乙、丙均为电解池 | |
| B. | 电子流动方向:电极Ⅳ→A→电极I | |
| C. | 当0.1mol电子转移时,电极I和电极Ⅳ的质量差为4.1g | |
| D. | 若丙中的电解质改为CuCl2,电极Ⅲ的电极反应发生改变 |
分析 电极Ⅰ为Al,其它均为Cu,Al易失电子作负极,所以Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,电流方向从正极流向负极,负极上失电子发生氧化反应,正极上得电子发生还原反应,据此分析解答.
解答 解:电极Ⅰ为Al,其它均为Cu,Al易失电子作负极,所以Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,
A.电极Ⅰ为Al,其它均为Cu,Al易失电子作负极,所以Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,所以甲乙构成原电池,丙为电解池,故A错误;
B.电子从负极沿导线流向正极,即电极Ⅰ→A→电极Ⅳ,故B错误;
C.Ⅰ是负极反应式为Al-3e-═Al 3+质量减少,电极Ⅳ是阴极,发生反应为Cu 2++2e-=Cu,质量增加,所以当0.1mol电子转移时,电极I和电极Ⅳ的质量差为$\frac{27}{3}$×0.1+$\frac{64}{2}$×0.1=4.1g,故C正确;
D.电极Ⅲ为阳极,电极反应式为Cu-2e-═Cu 2+,不受电解质溶液改变,故D错误;
故选C.
点评 本题考查了原电池原理,正确判断正负极是解本题关键,再结合各个电极上发生的反应来分析解答,题目难度中等.

练习册系列答案
相关题目
7.下列有机物命名正确的是( )
| A. |  2-甲基-2-氯丙烷 | B. | 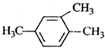 1,3,4-三甲苯 | C. | 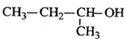 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 |
11.某学生为了探究锌与盐酸反应过程中的速率变化.在100mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如下:
(1)在0min~1min、1min~2min、2min~3min、3min~4min、4min~5min时间段中,反应速率最大的时间段是2~3min,原因该反应过程中放热使温度升高而加快反应速率,此时温度的影响起主要因素;反应速率最小的时间段是4~5min,原因为该反应过程中消耗H+使C H+减小而减慢反应速率,此时C H+的影响起主要因素.
(2)在2min~3min时间段内,用盐酸的浓度变化表示的反应速率为0.1mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.Na2SO4溶液 C.NaNO3溶液 D.Na2CO3溶液
你认为可行的是AB.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)在2min~3min时间段内,用盐酸的浓度变化表示的反应速率为0.1mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.Na2SO4溶液 C.NaNO3溶液 D.Na2CO3溶液
你认为可行的是AB.
1.向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述中正确的是( )
| A. | 钠熔化成小球 | |
| B. | 钠块沉在乙醇液面的下面 | |
| C. | 钠块在乙醇的液面上游动 | |
| D. | 钠块表面有气泡放出,有轻微爆炸产生 |
8.“钾泻盐”的化学式为MgSO4•KCl•xH2O,是一种制取钾肥的重要原料,它溶于水得到KCl与MgSO4的混合溶液.某化学活动小组设计了如下实验方案:以下说法不正确的是( )


| A. | 该方案能够计算出“钾泻盐”中KCl的质量分数 | |
| B. | 足量Ba(NO3)2溶液是为了与MgSO4充分反应 | |
| C. | “钾泻盐”化学式中x=3 | |
| D. | 上述实验数据的测定利用学校实验室里的托盘天平即可完成 |
20. 以NO、O2,熔融NaNO3,组成的燃料电池装置如图所示,在使用过程中石墨I生成NO2,Y为一种氧化物,下列说法不正确的是( )
以NO、O2,熔融NaNO3,组成的燃料电池装置如图所示,在使用过程中石墨I生成NO2,Y为一种氧化物,下列说法不正确的是( )
 以NO、O2,熔融NaNO3,组成的燃料电池装置如图所示,在使用过程中石墨I生成NO2,Y为一种氧化物,下列说法不正确的是( )
以NO、O2,熔融NaNO3,组成的燃料电池装置如图所示,在使用过程中石墨I生成NO2,Y为一种氧化物,下列说法不正确的是( )| A. | 石墨Ⅱ电极为正极 | |
| B. | Y为N2O5 | |
| C. | 石墨Ⅰ电极方程式为NO+O2--2e-=NO2 | |
| D. | 不能用NaNO3水溶液代替熔融NaNO3 |
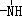 、
、 一定条件下都可以和H+结合.则N4和足量的H+反应生成的粒子的化学式为N4H44+.
一定条件下都可以和H+结合.则N4和足量的H+反应生成的粒子的化学式为N4H44+. 硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.