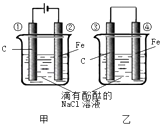
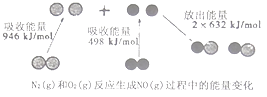
题目内容
【题目】图1为某套实验装置的示意图,其中加热装置和部分药品等均已省略(装置Ⅰ和装置Ⅱ为气体发生装置)。
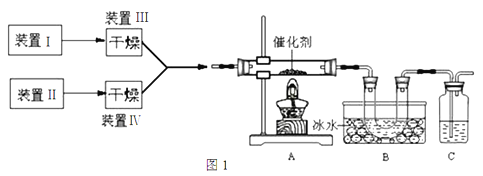
(1)甲同学用此装置(在A、B间增加一盛有浓硫酸的洗气瓶)
制备NO2并验证其性质。
①装置Ⅰ用于实验室制备NH3,装置Ⅱ制备过量O2。装置Ⅰ中发生反应的化学方程式为_____________________。
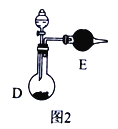
②也可以将制气体装置Ⅰ、Ⅱ、Ⅲ、Ⅳ合并为一个装置,如图2所示。若分液漏斗中盛装浓氨水,则D中的固体试剂为_______(填化学式),E中的试剂为____________。
(2)乙同学用此套装置合成SO3,B装置U形管中有固体出现。
①实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。 若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有25.0%的亚硫酸钠(质量分数)被氧化为硫酸钠,则至少需称取该亚硫酸钠的质量为______g(保留一位小数)。
②现欲制得纯净干燥的SO3,若图1装置C中盛放NaOH溶液,则此装置中存在明显不足:
a.C中的水蒸气可能进入B中与SO3反应;b.____________________________________。
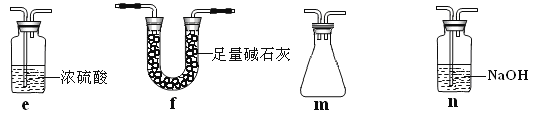
应如何改进:______________________________(从下图给出的实验装置中选择字母标号补充或替换,并用简要文字说明补充和替换的位置)。
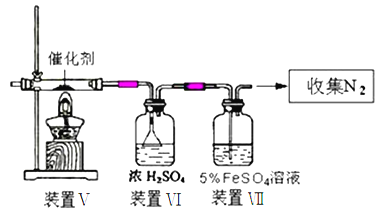
(3)丙同学拟验证NO能被氨气还原并测算其转化率(装置Ⅰ、装置Ⅱ分别制取NO和NH3),将图1装置中A、B、C分别换成图5中装置Ⅴ、Ⅵ、Ⅶ。
①写出氨气被NO氧化的化学方程式:___________________________。
②装置Ⅶ的作用可能是__________________________。
③若进入装置Ⅴ的NO共22.4L(已折算为标准状况,下同),氨气过量,最后收集到11.2LN2,则NO的转化率是__________________________。
【答案】 2NH 4 Cl+Ca(OH)2![]() CaCl 2 +2NH 3 +2H2O Na2O2 碱石灰 25.2 C中会发生倒吸现象 将C改为f装置 4NH3+6NO
CaCl 2 +2NH 3 +2H2O Na2O2 碱石灰 25.2 C中会发生倒吸现象 将C改为f装置 4NH3+6NO![]() 5N2+6H2O 吸收NO 60%
5N2+6H2O 吸收NO 60%
【解析】(1)①装置I用于实验室制备NH3,化学反应为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
②装置Ⅰ用于实验室制备NH3,装置Ⅱ制备过量O2,制备NO2并验证其性质,如果将可以将制气体装置Ⅰ、Ⅱ、Ⅲ、Ⅳ合并为一个装置,分液漏斗中盛装浓氨水,则D中的固体试剂为过氧化钠,过氧化钠与水反应放出氧气,同时反应放热,促使氨水分解放出氨气,氨的催化氧化需要干燥的气体反应,防止炸裂硬质玻璃管,因此E中的试剂为碱石灰,故答案为:Na2O2;碱石灰;
(2)①3.36L(标准状况)二氧化硫的物质的量为![]() =0.15mol,设该亚硫酸钠的质量为x,则
=0.15mol,设该亚硫酸钠的质量为x,则![]() =0.15mol,解得x=25.2g,故答案为:25.2;
=0.15mol,解得x=25.2g,故答案为:25.2;
②现欲制得纯净干燥的SO3,若图1装置C中盛放NaOH溶液,氢氧化钠溶液中的水蒸气会通过导管进入B中与SO3反应,三氧化硫与氢氧化钠反应容易产生倒吸现象,为了避免倒吸,可以将C改为f装置,故答案为:C中会发生倒吸现象;将C改为f装置;
(3)①氨气被NO氧化生成氮气和水,反应的化学方程式为4NH3+6NO![]() 5N2+6H2O,故答案为:4NH3+6NO
5N2+6H2O,故答案为:4NH3+6NO![]() 5N2+6H2O;
5N2+6H2O;
②装置I、装置II分别制NO和NH3,在V中二者发生氧化还原反应生成氮气,可能混有NO或氨气,装置Ⅵ可吸收水或氨气,因一氧化氮与二价铁形成配位键,溶液中淡绿色的二价铁变成棕色的一氧化氮配合物,反应为FeSO4+NO=Fe(NO)SO4,装置Ⅶ的作用吸收未反应的NO,故答案为:吸收NO;
③在一定条件下反应中气体的体积之比等于物质的量之比,
6NO+4NH3═5N2+6H2O
6 5
V 11.2L
![]() =
=![]() ,解得V=13.44L,则NO的转化率为
,解得V=13.44L,则NO的转化率为![]() ×100%=60%,故答案为:60%。
×100%=60%,故答案为:60%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案