题目内容
【题目】同温同压下有两份体积相同的CO2和O3 , 关于它们的叙述正确的是( )
A.分子数之比是1:1
B.原子个数比是3:2
C.质子数比是12:11
D.密度之比是1:1
【答案】A
【解析】解:同温同压下,气体摩尔体积相等,体积相同的CO2和O3的物质的量相等, A.根据N=nNA知,二者物质的量相等时,其分子数相等,故A正确;
B.二氧化碳和臭氧分子中原子个数相等,二者的分子数相等,则原子个数之比为1:1,故B错误;
C.二氧化碳和臭氧分子中质子数分别是22、24,其分子数相等,则质子数之比为22:24=11:12,故C错误;
D.根据ρ= ![]() 知,二者的密度之比等于其摩尔质量之比=44g/mol:48g/mol=11:12,故D错误;
知,二者的密度之比等于其摩尔质量之比=44g/mol:48g/mol=11:12,故D错误;
故选A.

 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
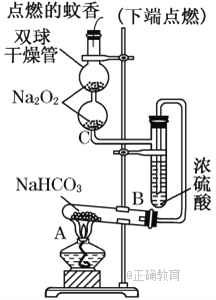
浙江之星学业水平测试系列答案【题目】火力发电在我国的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题,直接排放含SO2的烟气会形成酸雨,危害环境.
(1)用化学方程式表示SO2形成硫酸型酸雨的反应: .
(2)工业上用Na2SO3溶液吸收烟气中的SO2 . 将烟气通入1.0molL﹣1的Na2SO3溶液,溶液pH不断减小.当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂. ①此时溶液中c(SO32﹣)的浓度是0.2molL﹣1 , 则溶液中c(HSO3﹣)是molL﹣1 .
②向pH约为6的吸收剂中通入足量的O2 , 可将其中的NaHSO3转化为两种物质,反应的化学方程式是 .
③某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,模拟实验吸收含硫烟气,实验结果如图所示.则: , 有利于提高SO2的吸收效率.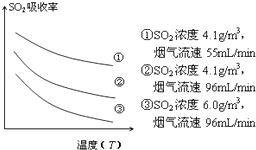
(3)工厂仓库存放的Na2SO3药品已部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定其含量,具体步骤如下: 步骤i称取样品1.000g.
步骤ii将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤iii移取25.00mL样品溶液于250mL锥形瓶中,用0.01000molL﹣1 KMnO4标准溶液滴定至终点.
按上述操作方法再重复2次.
①写出步骤iii所发生反应的离子方程式;
②在配制0.01000molL﹣1 KMnO4溶液时若仰视定容,则最终测得药品中Na2SO3的含量(填“偏大”、“偏小”或“无影响”).
③某同学设计用下列仪器进行滴定实验(夹持部分略去),最合理的组合是(填字母).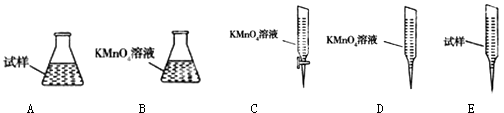
④滴定结果如下表所示:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 2.20 | 20.20 |
则该药品中Na2SO3的质量分数为 .