题目内容
6.苯甲酸甲酯是一种重要的工业原料,某研究性学习小组的同学拟用下列装置制取高纯度的苯甲酸甲酯.
有关数据如下表:
| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 水溶性 | |
| 苯甲酸 | 122.4 | 249 | 1.27 | 微溶 |
| 甲醇 | -97 | 64.3 | 0.79 | 互溶 |
| 苯甲酸甲酯 | -12.3 | 199.6 | 1.09 | 不溶 |
(1)在烧瓶中混合有机物及浓硫酸的方法是先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸,在实际实验中,甲醇、苯甲酸的物质的量之比远大于其理论上的物质的量之比,目的是提高苯甲酸的利用率.装置C中除甲醇、苯甲酸与浓硫酸外还需要放置沸石(或碎瓷片).
(2)C装置上部的冷凝管的主要作用是冷凝回流.
(3)制备和提纯苯甲酸甲酯的操作的先后顺序为(填装置字母代号)CFEADB.
(4)A装置锥形瓶中Na2CO3的作用是除去酯中的苯甲酸;D装置的作用是除去没有反应完的Na2CO3;当B装置中温度计显示199.6℃时可收集苯甲酸甲酯.
分析 本题是根据酯化反应原理合成苯甲酸甲酯,共分制备、提纯二个流程,涉及混合溶的配制及加热时防暴沸,液体混合物分离的二种常见分离方法分液和蒸馏操作的选择及适用对向的分析.
(1)有机物与浓硫酸的混合应可参考浓硫酸的稀释,酯化反应是可逆反应,通常通过增大反应的量来提高原料的利用率和产率,给加热液体混合物时,应防止液体暴沸;
(2)反应混合物加热产生的蒸汽要通过C装置上部的冷凝管冷凝重新回流反应容器中,减少原料的损耗,冷却水的水流方向采用逆流的方法,可提高与蒸汽的充分接触,便于冷却完全;
(3)在圆底烧瓶中加入0.1mol苯甲酸和0.4mol甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品;苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,需进行分液、蒸馏等操作;
(4)反应完全后有苯甲酸剩余需要通过添加Na2CO3与之反应除去,多余的碳酸钠微溶于有机混合物,可用过滤的方法分离,蒸馏时,根据苯甲酸甲酯的沸点确定温度;
解答 解:(1)参考浓硫酸的稀释,先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸来配制混合液,通过增加甲醇的量,提高苯甲酸的转化率,给液体混合物加热时通常添加沸石防暴沸,故答案为:先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸;提高苯甲酸的利用率;沸石(或碎瓷片);
(2)C装置上部的冷凝管可使反应混合加热时挥发出的蒸汽经冷凝重新回流反应容器中,减少原料的损耗,冷却水的水流方向与蒸汽的流向相反,选择从d口进入,c口流出,故答案为:冷凝回流;
(3)在圆底烧瓶中加入0.1mol苯甲酸和0.4mol甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品;苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,需进行分液、蒸馏等操作,可用分液的方法除去苯甲酸甲酯中的硫酸、苯甲酸,然后进行蒸馏,操作的顺序为CFEADB,故答案为:CFEADB;
(4)碳酸钠用于洗去苯甲酸甲酯中过量的酸,过量的碳酸钠用过滤的方法可除去,蒸馏时,将苯甲酸甲酯与甲醇、水分离,由苯甲酸甲酯的沸点可知应收集沸点199.6℃的馏分,故应控制温度199.6℃,故答案为:除去酯中的苯甲酸;除去没有反应的碳酸钠;199.6.
点评 本题考查有机物的合成,侧重对化学实验的考查,涉及对装置的理解、物质的分离提纯、对实验条件的控制、对数据的分析处理等,难度中等,需要学生基本知识的基础与灵活运用能力.

| A. | 32 | B. | 44 | C. | 46 | D. | 64 |
| A. | 体系的压强不再发生变化 | B. | 3v正(B)═2v逆(C) | ||
| C. | 混合气体密度不再变化 | D. | 消耗1molA的同时生成2molC |
| A. | 二氧化硫可广泛用于纸浆、毛、丝、草帽辫等的漂白 | |
| B. | 明矾净水的原理和“84”消毒液消毒的原理不相同 | |
| C. | 食醋可去除水垢,NH4Cl溶液可去除铁锈 | |
| D. | CO2和NO2都能使雨水的pH<5.6,导致酸雨的形成 |
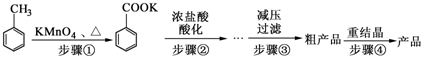
甲苯、苯甲酸钾、苯甲酸的部分物理性质见下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 在水中溶解性 |
| 甲苯 | -95 | 110.6 | 0.8669 | 难溶 |
| 苯甲酸钾 | 121.5~123.5 | 易溶 | ||
| 苯甲酸 | 122.4 | 248 | 1.2659 | 微溶 |
(2)步骤②用浓盐酸酸化的目的是使苯甲酸析出.
(3)减压过滤装置所包含的仪器除减压系统外,还有布氏漏斗、吸滤瓶(填仪器名称).
(4)已知温度越低苯甲酸的溶解度越小,但为了得到更多的苯甲酸晶体,重结晶时并非温度越低越好,理由是其它杂质也有可能析出.
(5)重结晶时需要趁热过滤,目的是为了减少苯甲酸的损失.
Ⅰ.脱硝:已知:H2的燃烧热为285.8kJ•mol-1
N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
H2O(g)=H2O(l)△H=-44kJ•mol-1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1.
Ⅱ.脱碳:向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H<0
(1)①下列叙述能说明此反应达到平衡状态的是de.
a.混合气体的平均摩尔质量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1molCO2生成的同时有3molH-H键断裂
②CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t4CO2的浓度随时间的变化.

(2)改变温度,使反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0中的所有物质都为气态.起始温度体积相同(T1℃、2L密闭容器).反应过程中部分数据见下表:
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ绝热恒容 | 0min | 0 | 0 | 2 | 2 |
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=0.025mol/(L.min);;在反应Ⅰ的条件下,该反应的平衡常数为$\frac{4}{27}$
③对反应Ⅰ,在其它条件不变,若30min时只改变一个条件,此时H2的物质的量浓度为1.6mol/L,则该条件可能为减少CO2的浓度,增大甲醇或水蒸气浓度,或升高温度.(写出两个情况即可)
④对反应Ⅰ,若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡不移动(填“正向”、“逆向”或“不”).
I.已知反应$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)△H=-23.5kJ•mol-1,该反应在1000℃的平衡常数等于4.在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡.
(1)CO的平衡转化率=60%
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是d.
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅱ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题:

(3)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=0.15mol/(L•min).
(4)已知氢气的燃烧热286kJ/mol,请写出甲醇气体不充分燃烧的热化学方程式CH3OH(g)+O2(g)=2H2O(l)+CO(g)△H=-481kJ/mol.
(5)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
A.c1=c2B.2Q1=Q3C.2α1=α3D.α1+α2=1E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量.
| A. | Cu2+、H+、Cl- | B. | Na+、CO32-、Cl- | C. | Na+、H+、Cl- | D. | Na+、OH-、CO32- |
| A. | 不需要加热就能发生的反应一定是放热反应 | |
| B. | 弱电解质溶液的导电能力一定比强电解质溶液的弱 | |
| C. | SO2溶于水,其水溶液能导电,故SO2是电解质 | |
| D. | 升高温度,可提高活化分子百分数,使有效碰撞增多,化学反应速率加快 |