题目内容
18.我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法.I.已知反应$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)△H=-23.5kJ•mol-1,该反应在1000℃的平衡常数等于4.在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡.
(1)CO的平衡转化率=60%
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是d.
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅱ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题:

(3)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=0.15mol/(L•min).
(4)已知氢气的燃烧热286kJ/mol,请写出甲醇气体不充分燃烧的热化学方程式CH3OH(g)+O2(g)=2H2O(l)+CO(g)△H=-481kJ/mol.
(5)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
A.c1=c2B.2Q1=Q3C.2α1=α3D.α1+α2=1E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量.
分析 I.(1)令平衡时CO的物质的量变化为nmol,利用三段式表示出平衡时CO、CO2的物质的量,化学计量数都是1,利用物质的量代替浓度代入平衡常数计算n的值,进而计算CO的浓度变化量,再利用转化率定义计算CO的转化率;
(2)a.该反应正反应是放热反应,提高反应温度,平衡向逆反应移动;
b.反应前后气体的物质的量不变,减小容器的容积,增大压强平衡不移动;
c.加入合适的催化剂,平衡不移动;
d.移出部分CO2,平衡向正反应移动;
e.粉碎矿石,使其与平衡混合气体充分接触,平衡不移动;
Ⅱ(3)根据v=$\frac{△c}{△t}$计算v(CH3OH),再利用速率之比等于化学计量数之比计算v(H2);
(4)氢气的燃烧热为286kJ/mol,则:2H2(g)+O2(g)=2H2O(l)△H=-572kJ/mol ①,
由图可得:CO(g)+2H2(g)?CH3OH(g)△H=-91kJ/mol ②,
根据盖斯定律,①-②可得:CH3OH(g)+O2(g)=2H2O(l)+CO(g);
(5)A.甲、乙是完全等效平衡,平衡时各组分的浓度相等;
B.丙与甲相比,等效为在甲平衡的基础上再加入1mol CO和2mol H2,压强增大,平衡向正反应方向移动,丙中反应物的转化率大于甲;
C.丙与甲相比,等效为在甲平衡的基础上再加入1mol CO和2mol H2,压强增大,平衡向正反应方向移动,后加入的1mol CO和2mol H2的转化率小于甲中的转化率;
D.CO的转化率为α1,则平衡时CO的物质的量为(1-α1)mol,乙中平衡时甲醇的转化率为α2,乙中平衡时CO的物质的量为α2mol,甲与乙是完全等效平衡,平衡时对应各组分的含量完全相同;
E.令平衡时CO的物质的量为nmol,CO(g)+2H2(g)?CH3OH(g)的反应热△H=-QkJ/mol,则Q1=(1-n)Q、Q2=nQ,整理得Q=Q1+Q2.
解答 解:I(1)令平衡时CO的物质的量变化为nmol,则:
$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)
开始(mol):1 1
变化(mol):n n
平衡(mol):1-n n+1
所以 $\frac{n+1}{1-n}$=4,解得n=0.6,则CO的平衡转化率为 $\frac{0.6mol}{1mol}$×100%=60%,
故答案为:60%;
(2)a.该反应正反应是放热反应,提高反应温度,平衡向逆反应移动,CO的平衡转化率降低,故a错误;
b.反应前后气体的物质的量不变,减小容器的容积,增大压强平衡不移动,CO的平衡转化率不变,故b错误;
c.加入合适的催化剂,平衡不移动,故c错误;
d.移出部分CO2,平衡向正反应移动,CO的平衡转化率增大,故d正确;
e.粉碎矿石,使其与平衡混合气体充分接触,可以加快反应速率,但平衡不移动,故e错误;
故答案为:d;
Ⅱ(3)由图可知,达到平衡时甲醇的浓度变化为0.75mol/L,则v(CH3OH)=$\frac{0.75mol/L}{10min}$=0.075mol/(L.min),速率之比等于化学计量数之比,v(H2)=2v(CH3OH)=0.15mol/(L•min),
故答案为:0.15mol/(L•min);
(4)氢气的燃烧热为286kJ/mol,则:2H2(g)+O2(g)=2H2O(l)△H=-572kJ/mol ①,
由图可得:CO(g)+2H2(g)?CH3OH(g)△H=-91kJ/mol ②,
根据盖斯定律,①-②可得:CH3OH(g)+O2(g)=2H2O(l)+CO(g),
则甲醇气体不充分燃烧的热化学方程式:CH3OH(g)+O2(g)=2H2O(l)+CO(g)△H=-481kJ/mol,
故答案为:CH3OH(g)+O2(g)=2H2O(l)+CO(g)△H=-481kJ/mol;
(5)A.甲、乙是完全等效平衡,平衡时各组分的浓度相等,所以平衡时甲醇的浓度c1=c2,故A正确;
B.丙与甲相比,等效为在甲平衡的基础上再加入1mol CO和2mol H2,压强增大,平衡向正反应方向移动,丙中反应物的转化率大于甲,丙中参加反应的CO大于甲中的2倍,故2Q1<Q3,故B错误;
C.丙与甲相比,等效为在甲平衡的基础上再加入1mol CO和2mol H2,压强增大,平衡向正反应方向移动,丙中反应物的转化率大于甲,后加入的1mol CO和2mol H2的转化率小于甲中的转化率,故2α1>α3 ,故C错误;
D.甲与乙是完全等效平衡,平衡时对应各组分的含量完全相同,CO的转化率为α1,则平衡时CO的物质的量为(1-α1)mol,乙中平衡时甲醇的转化率为α2,乙中平衡时CO的物质的量为α2mol,故(1-α1)=α2,整理得α1+α2=1,故D正确;
E.令平衡时CO的物质的量为nmol,CO(g)+2H2(g)?CH3OH(g)的反应热△H=-QkJ/mol,则Q1=(1-n)Q、Q2=nQ,整理得Q=Q1+Q2,故1mol CH3OH,则放出(Q1+Q2)kJ热量,故E正确,
故答案为:ADE.
点评 本题综合考查了化学平衡计算、等效平衡等,Ⅱ中等效平衡的计算,为该题的难点,也是易错点,注意理解等效平衡问题,题目整体计算量很大,思维量大,对学生的心理素质有很高的要求,难度较大.

| A. | 标况下,22.4L任何物质都含有约6.02×1023个分子 | |
| B. | NO的摩尔质量与6.02×1023个NO分子的质量相等 | |
| C. | 标况下,0.5×6.02×1023个一氧化碳分子所占体积为11.2L | |
| D. | 1molO2所含的分子数与12gC所含的原子数相等 |

有关数据如下表:
| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 水溶性 | |
| 苯甲酸 | 122.4 | 249 | 1.27 | 微溶 |
| 甲醇 | -97 | 64.3 | 0.79 | 互溶 |
| 苯甲酸甲酯 | -12.3 | 199.6 | 1.09 | 不溶 |
(1)在烧瓶中混合有机物及浓硫酸的方法是先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸,在实际实验中,甲醇、苯甲酸的物质的量之比远大于其理论上的物质的量之比,目的是提高苯甲酸的利用率.装置C中除甲醇、苯甲酸与浓硫酸外还需要放置沸石(或碎瓷片).
(2)C装置上部的冷凝管的主要作用是冷凝回流.
(3)制备和提纯苯甲酸甲酯的操作的先后顺序为(填装置字母代号)CFEADB.
(4)A装置锥形瓶中Na2CO3的作用是除去酯中的苯甲酸;D装置的作用是除去没有反应完的Na2CO3;当B装置中温度计显示199.6℃时可收集苯甲酸甲酯.
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 该温度下此反应的平衡常数K=144 | |
| C. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变 | |
| D. | 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) |
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2 反应情况 | 点燃时 易化合 | 加热化合 | 加热难 化合 | 不能直 接化合 |
(2)碲的化合价可能有-2,+4,+6.
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是H2Te>H2Se>H2S(填化学式).
(4)氢硒酸有较强的还原性(填“氧化性”或“还原性”).因此放在空气中长期保存易变质,其可能发生的化学方程式为2H2Se+O2=2H2O+2Se↓.
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:Al2Te3+6H2O----Al(OH)3↓+H2Te↑
| A. | 2-甲基丁烷和异戊烷 | B. | 分子量相同而结构不同的两种物质 | ||
| C. |  和 和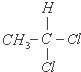 | D. | 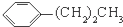 和 和 |
| 酸 | HX | HY | HZ |
| 电离常数K | 9×10-7 | 9×10-6 | 10-2 |
| A. | 三种酸的强弱关系:HX>HY>HZ | |
| B. | 反应HZ+Y-═HY+Z-能够发生 | |
| C. | 相同温度下,0.1 mol•L-1的HX、HY、HZ溶液,HX与锌反应一定最快 | |
| D. | 相同温度下,1 mol•L-1 HX溶液的电离常数大于0.1 mol•L-1 HX |
 向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m 与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法不正确的是( )
向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m 与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法不正确的是( )| A. | O→a时的反应的离子方程式为:Ba2++2OH-+SO42-+Mg2+═BaSO4↓+Mg(OH)2↓ | |
| B. | a→b时发生的离子反应为H++OH-=H2O | |
| C. | 从a→b→c说明溶液中结合OH-的能力强弱为:H+>Mg2+ | |
| D. | 原混合溶液中 C(HCl):C(MgSO4)=4:1 |
 某化学课外小组用如图装置制取溴苯.
某化学课外小组用如图装置制取溴苯.