题目内容
6.在某体系内有反应物和生成物5种物质:H2S、S、FeCl3、FeCl2、HCl.已知FeCl3为反应物,则另一反应物是( )| A. | FeCl2 | B. | H2S | C. | S | D. | HCl |
分析 已知FeCl3为反应物,则还原反应为FeCl3→FeCl2,Fe元素的化合价降低,该反应中S元素的化合价应升高,以此来解答.
解答 解:由信息可知,已知FeCl3为反应物,则还原反应为FeCl3→FeCl2,Fe元素的化合价降低,该反应中S元素的化合价应升高,可知氧化反应为H2S→S,则另一反应物为H2S,故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意利用化合价升降分析,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
17.下列关于卤素的叙述说法正确的是( )
| A. | 单质的颜色随核电荷数的增加逐渐加深 | |
| B. | 元素的最高化合价均为+7 | |
| C. | 从上到下原子半径递减 | |
| D. | 从上到下非金属的活拨性减弱 |
18. 有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
(1)D的离子结构示意图是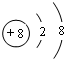 ;化合物Y所含的化学键名称离子键、共价键;B2C2的电子式表示为
;化合物Y所含的化学键名称离子键、共价键;B2C2的电子式表示为 .
.
(2)D、E、F的简单离子半径由大到小的顺序是(用化学式表示)S2->Cl->Al3+.
(3)写出两种均含A、B、C、F四种元素的化合物在溶液中相互反应的离子方程式H++HSO3-=SO2↑+H2O.
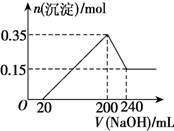
(4)将一定质量的Mg和D的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中Mg的质量为3.6g;原稀硫酸溶液的物质的量浓度为1mol/L.
 有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:| 元素编号 | 元素特征信息 |
| A | A的单质是密度最小的物质 |
| B | B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D与B同周期,该周期中D的简单离子半径最小 |
| E | B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F | F元素最高正价与最低负价的代数和为4 |
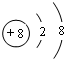 ;化合物Y所含的化学键名称离子键、共价键;B2C2的电子式表示为
;化合物Y所含的化学键名称离子键、共价键;B2C2的电子式表示为 .
.(2)D、E、F的简单离子半径由大到小的顺序是(用化学式表示)S2->Cl->Al3+.
(3)写出两种均含A、B、C、F四种元素的化合物在溶液中相互反应的离子方程式H++HSO3-=SO2↑+H2O.
(4)将一定质量的Mg和D的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中Mg的质量为3.6g;原稀硫酸溶液的物质的量浓度为1mol/L.
15.两个密闭容器:甲(定TV),乙(定TP),在甲、乙中各通入2molSO2和1mol O2,在相同的温度下达到如下平衡:2SO2(g)+O2(g)?2SO3(g),对此反应,下述说法不正确的是( )
| A. | 反应速率:乙>甲 | B. | SO2的转化率:乙>甲 | ||
| C. | 平衡时各组分含量:乙=甲 | D. | 平衡时容器的压强:乙>甲 |
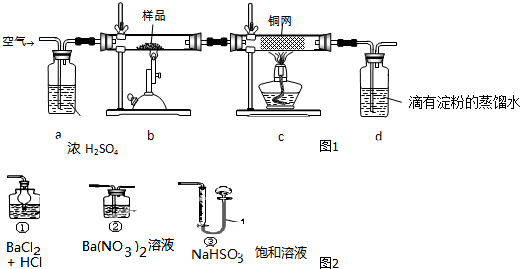
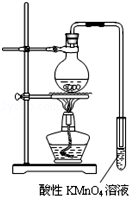 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.