题目内容
研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单的理解为断开1 mol 化学键时所需吸收的能量。下表是部分化学键的键能数据:
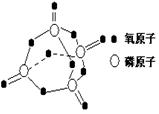
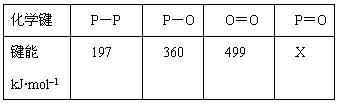
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图所示,则上表中X= kJ·mol–1。


已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图所示,则上表中X= kJ·mol–1。
433.75
略

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
 (g) △H=-25 KJ/mol
(g) △H=-25 KJ/mol 



 。
。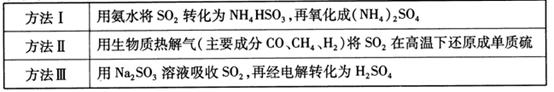
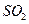 的化学反应为:
的化学反应为: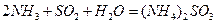
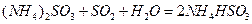
 . 通入空气使
. 通入空气使 转化为
转化为
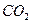 ,原因是▲(用离子方程式表示)。
,原因是▲(用离子方程式表示)。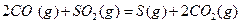
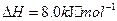
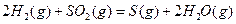
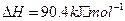
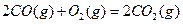
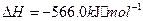
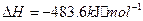
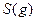 与
与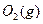 反应生成
反应生成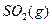 的热化学方程式为
的热化学方程式为  。
。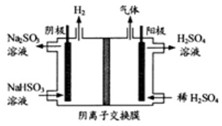
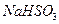 溶液的装置如上图所示。阳极区放出气体的成分为 。(填化学式)
溶液的装置如上图所示。阳极区放出气体的成分为 。(填化学式)