题目内容
已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-820KJ?mol-1.则下列说法中正确的是( )
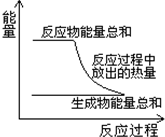
| A.反应过程中的能量变化关系可如图所示 |
| B.11.2LCH4完全燃烧放出热量410KJ |
| C.CH4的燃烧热为820KJ |
| D.凡是有水生成的氧化还原反应都是放热反应 |

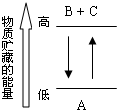
A、该反应的△H<0,从图象分析,反应物的能量高于生成物,反应是放热的,故A正确;
B、11.2L甲烷气体未必是0.5mol,因为只有在标准状况下Vm=22.4L/mol,0.5mol甲烷燃烧才能放出410KJ热量,故B错误;
C、燃烧热是指1mol可燃物燃烧生成液态水时放出的热量,本题生成的是水蒸气,故C错误;
D、氢气还原氧化铜有水生成,反应吸热,故D错误.
故选:A.
B、11.2L甲烷气体未必是0.5mol,因为只有在标准状况下Vm=22.4L/mol,0.5mol甲烷燃烧才能放出410KJ热量,故B错误;
C、燃烧热是指1mol可燃物燃烧生成液态水时放出的热量,本题生成的是水蒸气,故C错误;
D、氢气还原氧化铜有水生成,反应吸热,故D错误.
故选:A.

练习册系列答案
相关题目