题目内容
【题目】碳酸钠和碳酸氢钠广泛的应用于我们的生产和生活中。请回答下列问题。
(1)NaHCO3是膨松剂必不可少的成分,受热时能使面胚在焙烧过程中变得松软、多孔。写出受热时NaHCO3发生反应的化学方程式___。
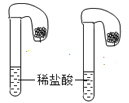
(2)请根据厨房中的物质,设计一实验鉴别某白色粉末是食盐还是食用碱(主要成分为Na2CO3)___。
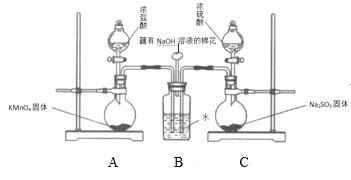
(3)如图是某兴趣学习小组设计的验证Na2CO3比NaHCO3热稳定性强的实验装置。

①乙处盛放固体药品的化学式是___;②变浑浊的是___烧杯中的澄清石灰水。
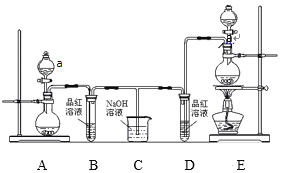
(4)兴趣学习小组为研究膨松剂在加热情况下放出气体的量,即:根据单位质量膨松剂产生CO2气体的量来判定其膨胀效果,设计了以下实验,并按如图装置连接(气密性良好,各装置中试剂均过量)。已知:浓硫酸常用于吸收水蒸气;碱石灰是固体氢氧化钠和氧化钙的混合物。回答下列问题:

①装置A中的作用为___。装置E的作用是___,
②如果去掉装置C,该实验会造成测定结果___(“偏大”、“不变”、“偏小”)
③加热前先通入一段时间的空气,再连接D装置,目的是___;停止加热后,还要继续通入一段时间的空气,这样做的目的是___。
【答案】2NaHCO3![]() Na2CO3+CO2↑+H2O 分别取未知的两种物质,然后分别加入食醋,有气体产生的为食用碱,无明显现象的为食盐 Na2CO3 丁 除去空气中的CO2 防止空气中的水蒸气和CO2与D中碱石灰反应 偏大 排净装置中的空气(CO2 ) 排净产生的CO2,让其被充分吸收
Na2CO3+CO2↑+H2O 分别取未知的两种物质,然后分别加入食醋,有气体产生的为食用碱,无明显现象的为食盐 Na2CO3 丁 除去空气中的CO2 防止空气中的水蒸气和CO2与D中碱石灰反应 偏大 排净装置中的空气(CO2 ) 排净产生的CO2,让其被充分吸收
【解析】
(1)受热时NaHCO3发生分解,生成碳酸钠、水和二氧化碳气体。
(2)鉴别某白色粉末是食盐还是食用碱(主要成分为Na2CO3),可使用厨房内的食醋,通过观察反应有无气泡产生,确定白色粉末的成分。
(3)①因为要确定Na2CO3比NaHCO3稳定,所以应给Na2CO3提供更高的温度,从而得出乙处盛放固体药品的成分。
(4)要想测定膨松剂的膨胀效果,必须使D装置中的碱石灰吸收分解产生的全部CO2,所以需将滞留在装置内的CO2全部排出,常使用不含CO2的空气。
①装置A中的作用为去除空气中的CO2。装置E的作用是防止空气中的某些成分进入E中而被吸收;
②如果去掉装置C,反应生成的水蒸气也会被碱石灰吸收,导致气体的质量增加;
③加热前先通入一段时间的空气,再连接D装置,目的是排尽装置内原有的空气;停止加热后,还要继续通入一段时间的空气,这样做的目的是将反应生成的CO2全部排出,让其被充分吸收。
(1)受热时NaHCO3发生分解,生成碳酸钠、水和二氧化碳气体,则受热时NaHCO3发生反应的化学方程式2NaHCO3![]() Na2CO3+CO2↑+H2O。答案为:2NaHCO3
Na2CO3+CO2↑+H2O。答案为:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(2)鉴别某白色粉末是食盐还是食用碱(主要成分为Na2CO3),可使用厨房内的食醋,通过观察反应有无气泡产生,确定白色粉末的成分。答案为:分别取未知的两种物质,然后分别加入食醋,有气体产生的为食用碱,无明显现象的为食盐;
(3)①因为要确定Na2CO3比NaHCO3稳定,所以应给Na2CO3提供更高的温度,乙处盛放固体药品的化学式是Na2CO3;②变浑浊的是丁烧杯中的澄清石灰水。答案为:Na2CO3;丁;
(4)要想测定膨松剂的膨胀效果,必须使D装置中的碱石灰吸收分解产生的全部CO2,所以需将滞留在装置内的CO2全部排出,常使用不含CO2的空气。
①装置A的作用为去除空气中的CO2。装置E的作用是防止空气中的水蒸气和二氧化碳进入E中而被吸收;答案为:除去空气中的CO2;防止空气中的水蒸气和CO2与D中碱石灰反应;
②如果去掉装置C,反应生成的水蒸气也会被碱石灰吸收,导致气体质量的增加,从而造成测定结果偏大;答案为:偏大;
③加热前先通入一段时间的空气,再连接D装置,目的是排尽装置内原有的空气;停止加热后,还要继续通入一段时间的空气,这样做的目的是将反应生成的CO2全部排出,让其被充分吸收。答案为:排净装置中的空气(CO2 );排净产生的CO2,让其被充分吸收。

 阅读快车系列答案
阅读快车系列答案