题目内容
【题目】乙二酸通常以二水合物的形式存在,俗称草酸晶体.已知草酸晶体在101℃时熔化并开始升华,157℃时大量升华,继续升温会分解生成CO、CO2和H2O。
(1)下列关于乙二酸的叙述正确的是(填编号)_____________
①能和乙二醇发生酯化反应
②能使酸性高锰酸钾溶液褪色
③其溶液能使蓝色石蕊试纸变红
④能和碳酸氢钠溶液反应生成气体
(2)乙二酸的工业生产方法之一是以乙二醇为原料,在一定条件下,用空气氧化得到.写出该反应的化学反应方程式:__________________________________
(3)欲检验草酸晶体受热分解的产物中是否有CO2,甲、乙两位同学分别设计了装置1、装置2来完成实验.
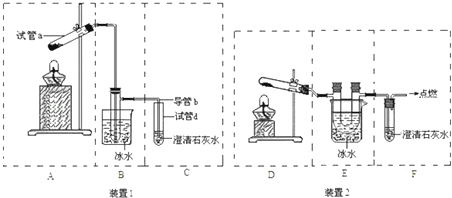
(Ⅰ)简述检验装置1气密性的操作方法:______________________________________
(Ⅱ)B和E两个装置中更合理的是______________
(Ⅲ)请从A~F中选择合适的仪器,组装一套可更好达到实验目的装置,按照气流由左到右的顺序依次为(用字母表示):________________.
(Ⅳ)一定条件下草酸氢铵分解生成NH3、CO、CO2和H2O,110℃时将该混合气体先通过Na2O2,再通过浓硫酸分别增重Ag和Bg; 若将混合气体先通过浓硫酸,再通过Na2O2分别增重Cg和Dg(能反应的气体均可吸收完全,且该条件下CO与Na2O2不反应),则A、B、C、D的大小关系为:______________
【答案】①②③④ 如图连接好装置,将导管b没入水中,微热(或手捂)试管a,看到导管口处有气泡冒出,撤火(或松手)后,观察到导管内有一段水柱上升,则说明该装置的气密性良好;EB中的导管过长、过细,冷凝后的乙二酸晶体可能会堵塞导管而存在安全隐患,E中采用U型管,与冰水的接触面积更大,更有利于乙二酸蒸气的冷凝,防止了乙二酸蒸气干扰CO2的检验A、E、F C>A>D>B
如图连接好装置,将导管b没入水中,微热(或手捂)试管a,看到导管口处有气泡冒出,撤火(或松手)后,观察到导管内有一段水柱上升,则说明该装置的气密性良好;EB中的导管过长、过细,冷凝后的乙二酸晶体可能会堵塞导管而存在安全隐患,E中采用U型管,与冰水的接触面积更大,更有利于乙二酸蒸气的冷凝,防止了乙二酸蒸气干扰CO2的检验A、E、F C>A>D>B
【解析】
(1)乙二酸分子中含有羧基,有酸性能发生酯化反应、能被高锰酸钾氧化;(2)乙二醇中含有羟基,能发生氧化反应,在一定条件下能被氧气氧化生成乙二酸;(3)装置气密性检验,先密闭装置,最后的导气管插入水中,微热后,有气泡冒出,冷却后导气管会有水柱上升,证明装置气密性完好;草酸晶体在101℃时熔化并开始升华,157℃时大量升华,试管中气体中含有草酸,需要除去,以免干扰CO2的检验;B中的导管过长、过细,冷凝后的乙二酸晶体可能会堵塞导管而存在安全隐患;E中采用U型管,与冰水的接触面积更大,更有利于乙二酸蒸气的冷凝,防止了乙二酸蒸气干扰CO2的检验;由于草酸在101℃时熔化,反应装置中试管口应向上倾斜,故选A装置;产生的气体中有草酸、一氧化碳,选择装置E除去草酸,一氧化碳有毒,具有可燃性,可采用点燃的方法除去尾气中的一氧化碳,二氧化碳能使澄清石灰水变浑浊,因此一般用澄清石灰水检验二氧化碳的存在,故选装置F;草酸氢铵受热分解生成二氧化碳、一氧化碳、氨气和水蒸气,混合气体先通过Na2O2,再通过浓硫酸,过氧化钠增重的Ag为二氧化碳、水总质量减去生成氧气的质量,浓硫酸增重的为氨气的质量,若将混合气体先通过浓硫酸,再通过Na2O2,浓硫酸增重为Cg为1mol水和1mol氨气的质量,过氧化钠增重的为1mol二氧化碳的质量减去生成氧气的质量,通过计算比较A、B、C、D的大小。
(1)乙二酸分子中含有羧基,具有酸性,且酸性比碳酸强,能使蓝色石蕊试液变红,能与碳酸氢钠反应生成二氧化碳;能与乙二醇发生发生酯化反应;能被酸性高锰酸钾氧化而使高锰酸钾溶液褪色,所以四个选项都正确,故答案为:①②③④;
(2)乙二醇中含有羟基,能发生氧化反应,在一定条件下能被氧气氧化生成乙二酸,化学方程式为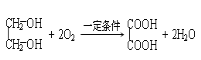 ,故答案为:
,故答案为: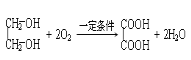 ;
;
(3)()检验装置1气密性的操作方法为:如图连接好装置,将导管b没入水中,微热(或手捂)试管a,看到导管口处有气泡冒出,撤火(或松手)后,观察到导管内有一段水柱上升,则说明该装置的气密性良好,故答案为:如图连接好装置,将导管b没入水中,微热(或手捂)试管a,看到导管口处有气泡冒出,撤火(或松手)后,观察到导管内有一段水柱上升,则说明该装置的气密性良好;
(Ⅱ)草酸晶体在101℃时熔化并开始升华,157℃时大量升华,试管中气体中含有草酸,需要除去,以免干扰CO2的检验;B中的导管过长、过细,冷凝后的乙二酸晶体可能会堵塞导管而存在安全隐患;E中采用U型管,与冰水的接触面积更大,更有利于乙二酸蒸气的冷凝,防止了乙二酸蒸气干扰CO2的检验,故答案为:E;B中的导管过长、过细,冷凝后的乙二酸晶体可能会堵塞导管而存在安全隐患;E中采用U型管,与冰水的接触面积更大,更有利于乙二酸蒸气的冷凝,防止了乙二酸蒸气干扰CO2的检验;
(Ⅲ)由于草酸在101℃时熔化,反应装置中试管口应向上倾斜,故选A装置;产生的气体中有草酸、一氧化碳,选择装置E除去草酸,一氧化碳有毒,具有可燃性,可采用点燃的方法除去尾气中的一氧化碳,二氧化碳能使澄清石灰水变浑浊,因此一般用澄清石灰水检验二氧化碳的存在,故选装置F;所有组装一套可更好达到实验目的装置,按照气流由左到右的顺序依次为:A、E、F,故答案为:A、E、F;
(Ⅳ)草酸氢铵分解生成NH3、CO、CO2和H2O:(NH4)HC2O4![]() NH3↑+CO↑+CO2↑+H2O↑,设草酸氢铵的物质的量为1mol,则完全分解生成的NH3、CO、CO2和H2O都是1mol;110℃时将该混合气体先通过Na2O2,再通过浓硫酸,过氧化钠增重Ag,浓硫酸增重Bg,过氧化钠增重的Ag为二氧化碳、水总质量减去生成氧气的质量,1mol水和1mol二氧化碳足量过氧化钠反应各生成0.5mol氧气,则:Ag=18g/mol×1mol+44g/mol×1mol
NH3↑+CO↑+CO2↑+H2O↑,设草酸氢铵的物质的量为1mol,则完全分解生成的NH3、CO、CO2和H2O都是1mol;110℃时将该混合气体先通过Na2O2,再通过浓硫酸,过氧化钠增重Ag,浓硫酸增重Bg,过氧化钠增重的Ag为二氧化碳、水总质量减去生成氧气的质量,1mol水和1mol二氧化碳足量过氧化钠反应各生成0.5mol氧气,则:Ag=18g/mol×1mol+44g/mol×1mol
﹣32g/mol×1mol=30g;浓硫酸增重的为1mol氨气的质量,则Bg=17g/mol×1mol=17g;若将混合气体先通过浓硫酸,再通过Na2O2,浓硫酸增重为Cg,过氧化钠增重为Dg,
浓硫酸增重为Cg为1mol水和1mol氨气的质量,则:Cg=18g+17g=35g;过氧化钠增重的为1mol二氧化碳的质量减去生成氧气的质量,1mol二氧化碳与足量过氧化钠反应生成0.5mol氧气,则Dg=44g﹣32g/mol×0.5mol=28g,所以A、B、C、D的大小关系为:C>A>D>B,故答案为:C>A>D>B。