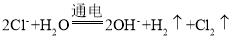题目内容
【题目】Ⅰ.如图是实验室制乙烯的发生装置和乙烯性质的实验装置,反应原理为CH3CH2OH![]() CH2=CH2↑+H2O,回答下列问题:
CH2=CH2↑+H2O,回答下列问题:

(1)图1中仪器①、②的名称分别为_______、_______。
(2)收集乙烯气体最好的方法是______________。
(3)向溴的四氯化碳溶液中通入乙烯(如图),溶液的颜色很快褪去,该反应属于_______(填反应类型),反应的化学方程式为______________。

Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。
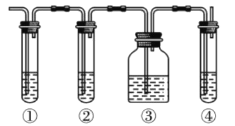
试回答下列问题:
(1)图中①、②、③、④装置盛放的试剂是下列中的(将正确选项填入空格内):
①_______;②_______;③_______;④_______。
A.氢氧化钠溶液 B.浓硫酸溶液 C.酸性高锰酸钾溶液 D.品红溶液
(2)能说明二氧化硫气体存在的现象是__________。
(3)使用装置②的目的是___________。
(4)使用装置③的目的是___________。
(5)确认含有乙烯的现象是__________。
【答案】温度计 圆底烧瓶 排水集气法 加成反应 CH2=CH2+Br2→CH2BrCH2Br D A D C ①中品红溶液褪色 吸收SO2 检验SO2是否被除尽 ③中品红溶液不褪色,④中KMnO4溶液褪色
【解析】
I.根据反应原理为CH3CH2OH![]() CH2=CH2↑+H2O,可知需要用温度计,结合乙烯的物理性质和化学性质分析解答;
CH2=CH2↑+H2O,可知需要用温度计,结合乙烯的物理性质和化学性质分析解答;
Ⅱ.二氧化硫为酸性气体,可与碱反应,具有漂白性,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,使酸性高锰酸钾溶液褪色;乙烯含有碳碳双键,能够与酸性高锰酸钾发生氧化还原反应,使酸性高锰酸钾溶液褪色,所以须先检验二氧化硫,然后除尽二氧化硫后再检验乙烯,据此分析解答。
I.(1)根据图示,图1中仪器①用于测量反应温度,为温度计;仪器②用于盛放乙醇和浓硫酸的混合液,为圆底烧瓶,故答案为:温度计;圆底烧瓶;
(2)乙烯的密度与空气密度接近,不能使用排空气法收集,乙烯不溶于水,可以用排水法水解乙烯,故答案为:排水集气法;
(3)向溴的四氯化碳溶液中通入乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,所以溶液的颜色很快褪去,反应的化学方程式为:CH2=CH2+Br2→CH2BrCH2Br,故答案为:加成反应;CH2=CH2+Br2→CH2BrCH2Br;
Ⅱ.(1)二氧化硫为酸性气体,可与碱反应;具有漂白性,可使品红褪色;具有还原性,可与酸性高锰酸钾发生氧化还原反应,使高锰酸钾褪色;乙烯含有碳碳双键,能够与酸性高锰酸钾发生氧化还原反应,使高锰酸钾褪色,所以须先检验二氧化硫,然后除尽二氧化硫后再检验乙烯。因此装置①中盛有品红溶液,用来检验二氧化硫的存在;然后将气体通入盛有氢氧化钠溶液的②中除去二氧化硫,再通入盛有品红溶液的③,确定二氧化硫是否除干净,最后通入盛有酸性高锰酸钾的④检验乙烯的存在,故答案为:D;A;D;C;
(2)二氧化硫具有漂白性,能够使品红溶液褪色,故答案为:①中品红溶液褪色;
(3)装置②中的NaOH溶液是用来除去SO2气体,以免干扰乙烯的检验,故答案为:吸收SO2;
(4)装置③中的品红溶液是检验SO2是否被除尽,防止二氧化硫干扰乙烯的检验,故答案为:检验SO2是否被除尽;
(5)装置③中的品红溶液不褪色可以排除二氧化硫的干扰,装置④中的酸性KMnO4溶液褪色,可证明乙烯的存在,故答案为:③中品红溶液不褪色,④中KMnO4溶液褪色。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
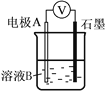
小学生10分钟应用题系列答案【题目】某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用下表中装置进行实验并记录。
装置 | 编号 | 电极A | 溶液B | 操作及现象 |
| Ⅰ | Fe | pH=2的H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_____________。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_______;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是___________。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
编号 | 溶液B | 操作及现象 |
Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是_____________。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究_____________________对O2氧化性的影响;实验Ⅳ中加入Na2SO4溶液的目的是_____________。