题目内容
17.亚硝酸钠是重要的防腐剂.某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠(夹持装置和A中加热装置已略,已密性已检验)
【查阅资料】
①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②在酸性溶液中,NO2可将MnO4还原为Mn2且无气体生产;
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸.
【实验操作】
①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;
③从C中取少量固体,检验是否是亚硝酸钠.
(1)A中反应的化学方程式是C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B中观察的主要现象是溶液变蓝,铜片溶解,导管口有无色气体冒出.
(3)检验C中产物有亚硝酸钠的实验方案(简述实验步骤、现象及结论)及相关的离子反应方程式为将生成物置于试管中,加入稀硫酸,若产生无色气体并在液面上方变为红棕色,则D中产物是亚硝酸钠.反应的离子方程式是3NO2-+2H+=NO3-+2NO↑+H2O,或将生成物置于试管中,加入酸性KMnO4溶液,若溶液紫色褪去,则D中产物是亚硝酸钠,反应的离子方程式是5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O.
(4)经检验C产物中亚硝酸钠含量较少.
a.甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠.生成碳酸钠的化学方程式是2CO2+2Na2O2═2Na2CO3+O2.为排除干扰,甲在B、C装置间增加一个U形管,U形管中盛放的试剂应是碱石灰(写名称).
b.乙同学认为上述装置改进后,还会有空气参与反应导致产品不纯,所以在实验操作①之前应增加一步操作,该操作是打开弹簧夹,通入N2一段时间.
分析 (1)装置A中是浓硝酸和碳加热发生的反应,反应生成二氧化氮和二氧化碳和水,依据氧化还原反应电子守恒和 原子守恒配平;
(2)装置B中是A装置生成的二氧化氮和水反应生成硝酸和一氧化氮,硝酸和铜反应生成硝酸铜,一氧化氮和水;
(3)依据亚硝酸钠具有氧化性或还原性,选择还原剂或氧化剂发生的反应现象证明产物中是否是亚硝酸钠;
(4)a、生成碳酸钠的反应是二氧化碳和过氧化钠发生的反应,生成碳酸钠和氧气;
b、为避免装置中的空气导致产品不纯,需要打开弹簧夹通入氮气排净装置中的空气.
解答 解:(1)装置A中是浓硝酸和碳加热发反应,反应生成二氧化氮和二氧化碳和水,反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(2)装置B中是A装置生成的二氧化氮和水反应生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,硝酸和铜反应生成硝酸铜,一氧化氮和水,所以反应现象为溶液变蓝,铜片溶解,导管口有无色气体冒出;通过装置C中的过氧化钠吸收一氧化氮、二氧化碳,最后通过酸性高锰酸钾溶液除去剩余一氧化氮防止污染空气,
故答案为:溶液变蓝,铜片溶解,导管口有无色气体冒出;除去未反应的NO,防止污染空气;
(3)检验亚硝酸钠的实验设计为将生成物置于试管中,加入稀硫酸,若产生无色气体并在液面上方变为红棕色,则D中产物是亚硝酸钠.反应的离子方程式是3NO2-+2H+=NO3-+2NO↑+H2O,或将生成物置于试管中,加入酸性KMnO4溶液,若溶液紫色褪去,则D中产物是亚硝酸钠,反应的离子方程式是5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O,
故答案为:将生成物置于试管中,加入稀硫酸,若产生无色气体并在液面上方变为红棕色,则D中产物是亚硝酸钠.反应的离子方程式是3NO2-+2H+=NO3-+2NO↑+H2O,或将生成物置于试管中,加入酸性KMnO4溶液,若溶液紫色褪去,则D中产物是亚硝酸钠,反应的离子方程式是5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O;
(4)a、生成碳酸钠的反应是二氧化碳和过氧化钠发生的反应,反应的化学方程式为:2CO2+2Na2O2═2Na2CO3+O2,通过装置C中的过氧化钠吸收一氧化氮、二氧化碳,一氧化氮是污染性气体,最后通过酸性高锰酸钾溶液除去剩余一氧化氮防止污染空气;为排除干扰在B、C装置间增加装置E,E中盛放的试剂应碱石灰,用来吸收二氧化碳;
故答案为:2CO2+2Na2O2═2Na2CO3+O2;碱石灰;
b.为避免装置中的空气导致产品不纯,需要打开弹簧夹通入氮气排净装置中的空气,
故答案为:打开弹簧夹,通入N2一段时间.
点评 本题考查了物质制备实验方案的设计和信息判断,物质性质的理解应用,注意实验过程中的反应现象分析,掌握基础是关键,题目难度中等.

| A. | 浓HCl | B. | 浓HN03 | C. | NaOH溶液 | D. | 稀HNO3 |

(1)连接好实验装置,检查装置的气密性,方法是关闭活塞K,微热反应管,试管A中有气泡冒出,停止加热,冷却后若末端导管中水柱上升且高度保持不变,说明气密性良好.
(2)制备氮化钙的操作步骤是:
①打开活塞K并通入N2;
②点燃酒精灯,进行反应;
③反应结束后,先熄灭酒精灯,待反应管冷却至室温,停止通N2并关闭活塞K;
④拆除装置,取出产物.
(3)数据记录如下:
| 空石英管质量 m0/g | 石英管与钙的质量 m1/g | 石英管与产物的质量 m2/g |
| 14.800 | 15.080 | 15.150 |
②上述实验产生误差的原因可能是AB (选填编号).
A.N2通入不足,反应器中有O2 B.钙与N2未充分反应 C.产物与空气接触.
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 | |
(1)下列四种离子结合质子的能力由大到小的顺序是a>b>d>c;(填编号)
a.CO32- b.ClO- c.CH3COO- d.HCO3-;
(2)下列反应不能发生的是:cd
a.CO32-+CH3COOH═CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH═CH3COO-+HClO
c.CO32-+HClO═CO2↑+H2O+ClO-
d.2ClO-+CO2+H2O═CO32-+2HClO
(3)用蒸馏水稀释0.10mol•L-1的醋酸,则下列各式表示的数值随水量的增加而增大的是B
A.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$ B.$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$
C.$\frac{c({H}^{+})}{{K}_{W}}$ D.$\frac{c({H}^{+})}{c(O{H}^{-})}$
(4)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程pH变化 如图甲,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数,稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液中水电离出来的c(H+)(填“大于”、“等于”或“小于”)

(5)向20mL硫酸和盐酸的混合溶液中,逐滴加入0.05mol•L-1Ba(OH)2溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图乙所示.计算:
①原混合溶液中c(H+)=0.3mol/L;c(Cl-)=0.2mol/L.
②A点的pH=1.
③将0.15mol•L-1稀硫酸V1mL与0.1mol•L-1NaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=1:1(溶液体积变化忽略不计).
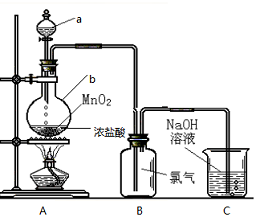 氯气的实验室制法
氯气的实验室制法

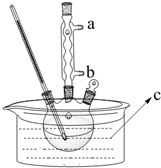 正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置来合成正丁醚(其它装置均略去),发生的主要反应为:
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置来合成正丁醚(其它装置均略去),发生的主要反应为: