题目内容
2.实验室里用如图所示装置制取纯净的无水CuCl2.试回答下列问题:
(1)写出A中圆底烧瓶中发生反应的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2 ↑+2H2O
(2)B处盛有饱和食盐水,其作用是除去Cl2中的HCl.
(3)C处盛放的试剂浓硫酸(填名称),其作用是干燥Cl2.
(4)E处盛有氢氧化钠溶液;发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(5)D处的反应方程式为:Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2
(6)实验结束时,应先熄灭D处酒精灯.
分析 利用装置A制备氯气,反应生成的氯气含有氯化氢和水蒸气,通过装置B中的饱和食盐水除去氯化氢气体,通过装置C中的浓硫酸除去水蒸气,得到干燥的氯气通过装置D和铜反应生成氯化铜,剩余氯气有毒,不能排到空气中,利用氯气和氢氧化钠溶液吸收,
(1)根据浓盐酸和二氧化锰的性质判断,二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水;
(2)浓盐酸的性质及反应方程式确定混合气体的成分,氯气中含氯化氢和水蒸气,氯化氢易溶于饱和食盐水;
(3)反应中的生成物含水蒸气,C处盛放的试剂是浓硫酸吸收水蒸气;
(4)氯气的性质确定尾气处理装置中物质,氯气是有毒气体不能排放到空气中污染空气;
(5)D中是干燥纯净的氯气和铜加热反应生成氯化铜;
(6)为避免温度降低,压强减小,溶液发生倒吸,依据防止倒吸分析;
解答 解:(1)浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水.
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2 ↑+2H2O.
(2)浓盐酸具有挥发性,所以混合气体中含有氯化氢;氯化氢极易溶于水,氯气的溶解度较小.所以可用盛有饱和食盐水除去混合气体中的氯化氢.
故答案为:饱和食盐水,除去Cl2中的HCl.
(3)因为题中要求制取纯净的无水CuCl2,所以要除去氯气中混有的水蒸气,且不引进新的杂质、氯气也和该物质不反应,所以该物质起干燥作用.
故答案为:浓硫酸;干燥Cl2.
(4)氯气有毒,所以不能直接排空,氯气和水能反应生成酸,酸和碱反应,所以可用碱液吸收氯气,氯气和碱反应生成盐、次氯酸盐、水.
故答案为:氢氧化钠溶液;Cl2+2OH-=Cl-+ClO-+H2O;
(5)D处是干燥纯净的氯气和铜加热反应生成氯化铜,反应的化学方程式为:Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2.
故答案为:Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2.
(6)为防止倒吸应先熄灭D的酒精灯,冷却再熄灭A的酒精灯,故答案为:D.
点评 本题有一定的综合性,把氯气的实验室制法和氯气的化学性质结合起来.考查学生对实验原理、实验装置的理解、物质的制备与性质,难度中等,实验室制取氯气的注意事项:1、必须用浓盐酸,稀盐酸不反应.2、为了减少制得的氯气中氯化氢的含量,所以加热温度不宜过高,浓盐酸具有挥发性.3、实验结束后,先使反应停止并排出残留的氯气,再拆卸装置,避免污染空气.4、尾气吸收时,不能用澄清石灰水吸收氯气,因为溶液中含有氢氧化钙的量少,吸收不完全.

| A. | KCl溶液 | B. | CH3CH2OH溶液 | C. | CH3COOH溶液 | D. | NaOH溶液 |
CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2+H2OCH2=CH2Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据如右:
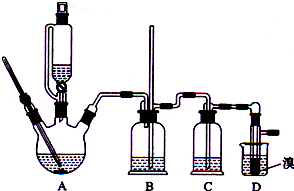
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母,下同)
a.引发反应 b.加快反应速度 c.防止乙醇挥发d.减少副产物乙醚生成
(2)反应过程中A装置可能产生的酸性干扰气体SO2(填化学式),为此在装置C中应加入c(从下列选项中选择)以吸收除杂.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.高锰酸钾溶液
(3)装置B是安全瓶,其工作原理是当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大.
(4)若产物中有少量未反应的Br2,最好用下列试剂中的c洗涤(填选项符号),再通过分液的方法分离;
a.水 b.氢氧化钠溶液 c.NaHSO3溶液 d.苯
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去;
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
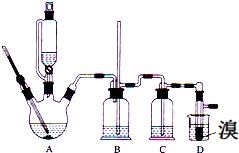 实验室用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的装置如图所示,其中可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
实验室用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的装置如图所示,其中可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的两步反应方程式为C2H5OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O、CH2=CH2+Br2→CH2BrCH2Br.
(2)在此实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰
水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
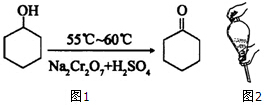 环己酮是一种重要的有机化工原料.实验室合成环己酮的反应如图1:
环己酮是一种重要的有机化工原料.实验室合成环己酮的反应如图1:环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3、20℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
a.蒸馏、除去乙醚后,收集151℃~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量水
回答下列问题:
(1)上述分提纯步骤的正确顺序是d b e c a.
(2)b中水层用乙醚萃取的目的是使水层中残留有机物进一步被提取,提高产品产量.
(3)以下关于萃取分液操作的叙述中,不正确的是ABC.
A.水溶液中加入乙醚,转移至分液漏斗,塞上玻璃塞,如图2用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分漏斗静置液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是降低环己酮的溶解度,增加水层的密度,有利于分层.
(5)蒸馏除乙醚的操作中采用的加热方式为水浴加热.收集产品时,实验制得的环己酮质量低于理论产量,可能的原因是C
A.蒸馏时从151℃开始收集产品 B.环己醇实际用量过多 C.制备粗品时环己醇有损失
(6)恢复至室温时,分离得到纯产品体积为12mL,则环己酮的产率约是60.3%.(保留小数点后1位数)





