��Ŀ����
4��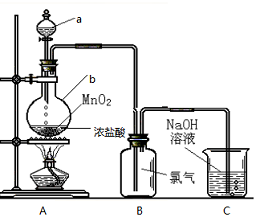 ������ʵ�����Ʒ�
������ʵ�����Ʒ���ʵ����������������Ũ�����MnO2�ڼ��������·�Ӧ����ȡ��ʵ������ȡ�����Ļ�ѧ����ʽ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
����������Ӧԭ���������������ͼʵ��װ�ã�����ʵ�����Ʊ�������Cl2��
��1��ʵ��������a����Һ©���� b��Բ����ƿ��
��2��������װ����������
A�����ķ���װ�ã�B�����ռ�װ�ã�����Cl2�ܶȱȿ����ܶȴ����ܣ���ܡ����ܡ�������ˮ�������ڱ���ʳ�Σ����������ſ��������ű���ʳ��ˮ���ռ�������C��β������װ�ã���Cl2�ж���Ⱦ������������������Һ��ȡ�����������
���� ���ݷ�Ӧԭ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O���н��
��1�����ݳ��������Ĺ����ж�����a��b�����ƣ�
��2������ͼʾװ���ص��ж������ã��������������������ж��������ռ����������������Ļ�ѧ�����ж�β�������Լ���
��� �⣺ʵ��������Ũ��������������ڼ��������·�Ӧ�����������÷�Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��Ũ���MnO2�����ȣ�MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��1������ͼʾװ�ÿ�֪������aΪ��Һ©��������bΪԲ����ƿ��
�ʴ�Ϊ����Һ©����Բ����ƿ��
��2��װ��A�ж���������Ũ�����ڼ��������·�Ӧ��������������A������������������װ��BΪ�����ռ�װ�ã����������ܹ�����ˮ������ֱ������ˮ���ռ����ɸ������������ڱ���ʳ��ˮ�����ű���ʳ��ˮ���ռ����������ܶȴ��ڿ�����Ҳ�����������ſ������ռ�������
�����ж����������������ֱ���ŷţ���Ҫ�õ�Cβ������װ�ã������ܹ����Һ��Ӧ����������������Һ���ն����������
�ʴ�Ϊ�������ķ����������ռ������ܣ������ſ������ű���ʳ��ˮ��β�����գ�����������Һ��
���� ���⿼����������ʵ�����Ʒ������ʣ���Ŀ�Ѷ��еȣ���ȷ�������Ʊ�ԭ�������е��������ʡ���ѧ����Ϊ���ؼ���������ػ���֪ʶ�Ŀ��飬������ѧ���ķ�����������ѧʵ��������

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�| A�� | ��������ά����C����ǿ�Դ�Ⱦ���ĵֿ��������������нⶾ���� | |
| B�� | ά����D���ڵ��͵�ˮ����ά���� | |
| C�� | Ϊ���������߲��е�ά����C����ʧ�����߲˵�ʱ�䲻��̫�������켴�� | |
| D�� | ����ά����D����������Ƶ����� |
| A�� | H2������Cl2��ȼ�� | B�� | �������õ�H2 | ||
| C�� | NaOH������ | D�� | Cl2����������Ư�� |
| A�� | ��Һ�и����ӵ�Ũ�ȶ���С | B�� | c��Cl-��/c��NH4+����С | ||
| C�� | c��H+��/c��NH4+������ | D�� | c��H+��•c��OH-����С |
| A�� | Fe+2HCl�TH2��+FeCl2 | B�� | 2FeCl2+Cl2 �T2FeCl3 | ||
| C�� | CaO+H2O�TCa��OH��2 | D�� | 2Fe��OH��3 $\frac{\underline{\;��\;}}{\;}$Fe2O3+3H2O |
CH3CH2CH2CH2OH$��_{H_{2}SO_{4}����}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
��Ӧ��Ͳ������������б����£�
| �е�/�� | �ܶ�/��g•cm-3�� | ˮ���ܽ��� | |
| ������ | 11.72 | 0.8109 | �� |
| ����ȩ | 75.7 | 0.8017 | �� |
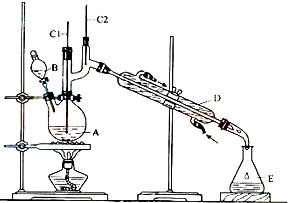
��6.0g Na2Cr2O7����100mL�ձ��У���30mLˮ�ܽ⣬�ٻ�������5mLŨ���ᣬ��������ҺС��ת����B�У���A�м���4.0g�������ͼ�����ʯ�����ȣ�������������ʱ����ʼ�μ�B����Һ���μӹ����б��ַ�Ӧ�¶�Ϊ90-95�棬��E���ռ�90�����µ���֣�
������ﵹ���Һ©���У���ȥˮ�㣬�л������������ռ�75-77����֣�����2.0g��
�ش��������⣺
��1��ʵ���У��ܷ�Na2Cr2O7��Һ�ӵ�Ũ�����У�˵�����ɲ��ܣ��������Ž���
��2�������ʯ�������Ƿ�ֹ���У�
��3������װ��ͼ�У�B�����������Ƿ�Һ©����D������������ֱ�������ܣ�
��4����Һ©��ʹ��ǰ������еIJ�����c������ȷ�𰸱�ţ���
a����ʪb������ c����© d���궨
��5��������ȩ�ֲ�Ʒ���ڷ�Һ©���з�ˮʱ��ˮ���²㣨��ϡ����¡���
��6����Ӧ�¶�Ӧ������90-95�棬��ԭ���DZ�֤����ȩ��ʱ�������ֿɾ��������䱻��һ��������
��7����ʵ���У�����ȩ�IJ���Ϊ51.4%��
