题目内容
如图是元素周期表的一部分,下列说法正确的是( )
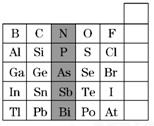

| A、阴影部分元素在周期表中处于第ⅣA族 |
| B、H3AsO4的酸性大于H3PO4 |
| C、元素铊(Tl)的最高价氧化物的水化物的碱性:Tl(OH)3<Al(OH)3 |
| D、元素砹(At)为有色固体,难与氢气化合 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.主族元素族序数与其原子最外层电子数相等;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强;
D.同一主族元素,元素的非金属性随着原子序数增大而减弱,非金属性越强,其单质与氢气越容易化合;第VIIA族元素单质其颜色随着原子序数增大而加深.
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强;
D.同一主族元素,元素的非金属性随着原子序数增大而减弱,非金属性越强,其单质与氢气越容易化合;第VIIA族元素单质其颜色随着原子序数增大而加深.
解答:
解:A.阴影部分元素最外层电子数为5,在周期表中处于第VA族,故A错误;
B.非金属性P>As,所以酸性H3PO4较大,故B错误;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强H3AsO4的酸性小于H3PO4,故C错误;
D.非金属性I>At,与氢气化合容易程度I>At,卤族元素单质随着原子序数增大而颜色加深,所以元素砹(At)为有色固体,难与氢气化合,故D正确;
故选D.
B.非金属性P>As,所以酸性H3PO4较大,故B错误;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强H3AsO4的酸性小于H3PO4,故C错误;
D.非金属性I>At,与氢气化合容易程度I>At,卤族元素单质随着原子序数增大而颜色加深,所以元素砹(At)为有色固体,难与氢气化合,故D正确;
故选D.
点评:本题考查了元素周期表和元素周期律的综合应用,明确同一周期、同一主族元素周期律内涵即可解答,题目难度不大.

练习册系列答案
相关题目
下列能够通过催化加氢后得到2、3-二甲基丁烷的是( )
| A、2、3-二甲基-1-丁烯 |
| B、2、3-二甲基-1-丁炔 |
| C、2、3-二甲基-1、3丁二烯 |
| D、2、3-二甲基-2-丁炔 |
对于平衡:2A+2B?C+2D+3E+H2O(A、B、C、D、E为溶液中可自由移动的微粒),下列判断正确的是( )
| A、加水平衡左移 |
| B、增加A,可提高B的转化率 |
| C、平衡后,按起始投料比,再次投入A和B,则A和B的转化率都将增大 |
| D、升温该平衡一定发生移动 |
高铁酸钠(Na2FeO4)是一种新型的净水剂,对河湖水消毒,是城市饮水处理的新技术,制取Na2FeO4的反应为:Fe2O3+3Na2O2═2Na2FeO4+Na2O,下列说法不正确的是( )
| A、Fe2O3是反应的还原剂 |
| B、此反应中3mol Na2O2转移电子数3mol |
| C、Na2FeO4反应的氧化产物 |
| D、Na2FeO4能消毒杀菌是因其具有强氧化性 |
X、Y、Z为三种短周期元素,X、Y同周期,X、Z的最低价离子分别为X2-、Z-,Y2+与Z-具有相同的电子层结构,下列叙述一定不正确的是( )
| A、它们的原子序数X>Y>Z |
| B、原子最外层上的电子数Z>X>Y |
| C、Z的单质可以从NaBr溶液中置换出Br2 |
| D、X的最高价氧化物对应水化物是强酸 |
下列反应的离子方程式正确的是( )
| A、碳酸氢铵溶液与足量氢氧化钠溶液反应并加热NH4++OH-═NH3↑+H2O |
| B、氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
| C、Fe2O3固体溶于过量氢碘酸溶液中:Fe2O3+6H+═2Fe3++3H2O |
| D、苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
某些食品包装盒中有一个小袋,袋上注明“双吸剂,不可食用”,通过上网查询得知其主要成分是铁粉、活性炭和氯化钠”.关于这种双吸剂的分析判断错误的是( )
| A、具有抗氧化作用 |
| B、可吸收食品盒内的O2和N2 |
| C、发挥作用时利用了原电池原理 |
| D、变为红褐色后失效 |