题目内容
高铁酸钠(Na2FeO4)是一种新型的净水剂,对河湖水消毒,是城市饮水处理的新技术,制取Na2FeO4的反应为:Fe2O3+3Na2O2═2Na2FeO4+Na2O,下列说法不正确的是( )
| A、Fe2O3是反应的还原剂 |
| B、此反应中3mol Na2O2转移电子数3mol |
| C、Na2FeO4反应的氧化产物 |
| D、Na2FeO4能消毒杀菌是因其具有强氧化性 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:Fe2O3+3Na2O2═2Na2FeO4+Na2O中,Fe元素的化合价由+3价升高为+6价,过氧化钠中O元素的化合价由-1价降低为-2价,以此来解答.
解答:
解:A.Fe元素的化合价升高,则Fe2O3是反应的还原剂,故A正确;
B.此反应中3mol Na2O2转移电子数3mol×2×[(-1)-(-2)]=6mol,故B错误;
C.Fe元素的化合价升高被氧化,则Na2FeO4反应的氧化产物,故C正确;
D.Na2FeO4能消毒杀菌,含+6价的铁,具有强氧化性,故D正确;
故选B.
B.此反应中3mol Na2O2转移电子数3mol×2×[(-1)-(-2)]=6mol,故B错误;
C.Fe元素的化合价升高被氧化,则Na2FeO4反应的氧化产物,故C正确;
D.Na2FeO4能消毒杀菌,含+6价的铁,具有强氧化性,故D正确;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关铁元素的叙述中正确的是( )
| A、铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| B、氢氧化铁可以由相应的物质通过化合反应而制得 |
| C、氢氧化铁与氢碘酸反应:Fe(OH)3+3HI═FeI3+3H2O |
| D、铁元素位于周期表中第4周期第VIIIB族 |
下列说法正确的是( )
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质 |
| C、Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| D、碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物 |
如图是元素周期表的一部分,下列说法正确的是( )
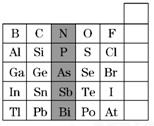

| A、阴影部分元素在周期表中处于第ⅣA族 |
| B、H3AsO4的酸性大于H3PO4 |
| C、元素铊(Tl)的最高价氧化物的水化物的碱性:Tl(OH)3<Al(OH)3 |
| D、元素砹(At)为有色固体,难与氢气化合 |
桶烯(Barrelene)结构简式如图所示,有关说法不正确的是( )
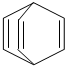

| A、桶烯分子中所有原子不可能在同一平面内 |
| B、桶烯在一定条件下能发生加成反应 |
| C、桶烯的分子式C8H8 |
| D、桶烯的一个氢原子被Cl取代,有四种结构 |
下列溶液一定呈中性的是( )
| A、pH=7的溶液 |
| B、c(H+)=c(OH-)的溶液 |
| C、滴加酚酞,颜色未变红的溶液 |
| D、酸与碱恰好完全反应生成正盐的溶液 |
下列设备工作时,将化学能转化为电能的是( )
A、硅太阳能电池 |
B、锂离子电池 |
C、太阳能集热器 |
D、燃气灶 |
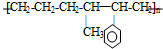 的单体的结构简式:
的单体的结构简式: