题目内容
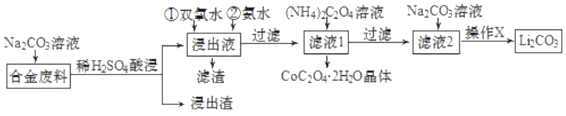
【题目】含有Cu、Fe、Al、Co、Li、Si等成分的某合金废料回收利用的工艺流程如图所示。
已知:
①Fe、Co在周期表中属同周期、同族;常温下,pH=7.3时Li+或Co3+开始沉淀。
②有关物质的溶度积(Ksp):
物质 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
Ksp | 4.0×10-21mol3·L-3 | 1.0×10-32mol4·L-4 | 1.0×10-38mol4·L-4 | 8.0×10-19mol3·L-3 |
回答下列问题
(1)Na2CO3溶液可作为合金废料的油污除剂,用离子方程式表示其原理__。
(2)“浸出渣”中的物质为__。
(3)①“浸出液”加入双氧水的作用是__(用离子方程式表示)。
②氨水的作用是调节溶液的pH,常温下,使溶液中杂质离子刚好沉淀完全而全部除去(浓度小于1.0×10-5mol·L-1认为完全沉淀)。需调节溶液的pH范围为__。
(4)得到的CoC2O4·2H2O晶体在空气中充分焙烧可得Co2O3,化学方程式为__。
(5)已知Li2CO3微溶于水,其饱和溶液的浓度与温度的关系如表所示。
温度/℃ | 10 | 30 | 60 |
浓度/(mol·L-1) | 0.21 | 0.17 | 0.14 |
则操作X为蒸发浓缩、__,理由是__。
【答案】CO32-+H2O![]() HCO3-+OH- Cu、Si 2Fe2++H2O2+2H+=2Fe3++2H2O 5.0<pH<7.3 4CoC2O4·2H2O+3O2
HCO3-+OH- Cu、Si 2Fe2++H2O2+2H+=2Fe3++2H2O 5.0<pH<7.3 4CoC2O4·2H2O+3O2![]() 2Co2O3+8H2O+8CO2 趁热过滤 减少Li2CO3的溶解损失
2Co2O3+8H2O+8CO2 趁热过滤 减少Li2CO3的溶解损失
【解析】
合金废料(含有Cu、Fe、Al、Co、Li、Si)加入碳酸钠溶液除去合金废料的油污,加入稀硫酸,浸出渣含有铜、硅,浸出液中加入过氧化氢氧化亚铁离子为铁离子,加入氨水调节溶液pH使铁离子转化为氢氧化铁沉淀、铝离子转化为氢氧化铝沉淀,通过过滤得到溶液1中加入草酸铵溶液沉淀钴离子,过滤得到溶液2主要是锂离子的溶液,加入碳酸钠沉淀锂离子,过滤得到碳酸锂,以此解答该题。
(1)Na2CO3溶液中存在水解平衡:CO32-+H2O![]() HCO3-+OH-,溶液显碱性,与油脂发生水解反应,能去除油污;;
HCO3-+OH-,溶液显碱性,与油脂发生水解反应,能去除油污;;
(2)铜、硅与稀硫酸不反应,则浸出渣含有铜、硅;
(3)①加入H2O2的作用是氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②使溶液中杂质离子刚好沉淀完全而全部除去(浓度小于1.0×10-5molL-1),由于Ksp[Al(OH)3]>Ksp[Fe(OH)3],当铝离子沉淀完全时,铁离子已经沉淀完全,所以根据Ksp[Al(OH)3]=c3(OH-)c(Al3+)可知c(OH-)=![]() =1×10-9molL-1,所以此时溶液的pH值为5,同时要使Li+或Co3+不沉淀,则pH<7.3,所以要调节溶液的pH值为5.0<pH<7.3,
=1×10-9molL-1,所以此时溶液的pH值为5,同时要使Li+或Co3+不沉淀,则pH<7.3,所以要调节溶液的pH值为5.0<pH<7.3,
故答案为:5.0<pH<7.3;
(4)CoC2O4晶体焙烧生成Co2O3、CO2和水,反应的化学方程式为4CoC2O42H2O+3O2![]() 2Co2O3+8 H2O+8CO2;
2Co2O3+8 H2O+8CO2;
(5)Li2CO3微溶于水,溶解度随温度升高而降低,为减少Li2CO3的溶解损失,蒸发浓缩后必须趁热过滤,

 阅读快车系列答案
阅读快车系列答案【题目】钒及其化合物在工业上有许多用途。某钒精矿的主要成分及质量分数如下表:
物质 | V2O5 | V2O3 | K2O | SiO2 | Fe2O3 | Al2O3 |
质量分数% | 0.81 | 1.70 | 2.11 | 63.91 | 5.86 | 12.51 |
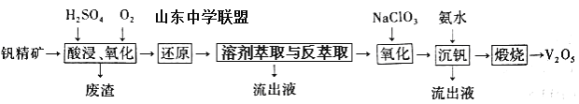
一种从该钒精矿中提取五氧化二钒的流程如下:
回答下列问题:
(1)“酸浸、氧化”时,V2O3转化为VO2+,反应的离子方程式为____________________________________;若用浓盐酸代替硫酸,V2O5转化为VO2+,同时生成有毒的黄绿色气体,反应的化学方程式为__________________。
(2)萃取剂对四价钒具有高选择性,且萃取Fe3+而不萃取Fe2+,所以萃取前可用____________(填名称,下同)对浸出液进行“还原”处理。为检验“还原”后的滤液中是否含有Fe3+,可选用的化学试剂是____________________。
(3)“溶剂萃取与反萃取”可表示为:VO2+ + (HR2PO4)2(O)![]() VO(R2PO4)2(O)+ 2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈 __________性(填“酸”“碱”或“中”)。
VO(R2PO4)2(O)+ 2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈 __________性(填“酸”“碱”或“中”)。
(4)“氧化”中,欲使3molVO2+变为VO2+,则需要氧化剂NaClO3至少为____________mol。
(5)单质钒可用于制造特种合金钢。以五氧化二钒和金属钙为原料在高温条件下可制备单质钒,表示制备过程的化学方程式为________________________________________。