��Ŀ����
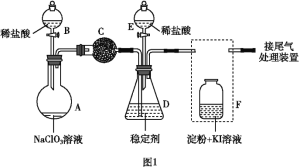
����Ŀ��ClO2(����ɫ������ˮ������)��һ�ָ�Ч���Ͷ�����������ij��ȤС��ͨ��ͼ1װ��(�г�װ����)�����Ʊ������պ��ͷŽ������о���
(1)����A��������_______________________��
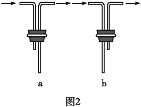
(2)��װF�е���ʱ��Ӧѡ��ͼ2�е�___________________��
(3)A�з�����Ӧ����ClO2��Cl2������������ͻ�ԭ�������ʵ���֮��Ϊ__________��
(4)�ر�B�Ļ�����ClO2��D�б��ȶ�����ȫ��������NaClO2����ʱF����Һ����ɫ���䣬��װ��C��������__________________��
(5)��֪������������NaClO2�ɷ�����Ӧ����NaCl���ͷų�ClO2���÷�Ӧ�����ӷ���ʽΪ____��
(6)ClO2�ܲ��ȶ������������ƣ�������ˮ���տɵõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2��Ũ�ȣ�����������ʵ�飺
����1��ȷ��ȡClO2��Һ10.00mL��ϡ�ͳ�100.00mL��������ȡV0 mL�������뵽��ƿ�У�
����2����ϡ�������������pH��2.0������������KI���壬����Ƭ�̣�
����3������ָʾ������c mol��L1 Na2S2O3��Һ�ζ����յ㡣�ظ�2�Σ��������Na2S2O3��Һƽ��ֵΪV1 mL��
(��֪2ClO2+10I+8H+=2Cl+5I2+4H2O��2Na2S2O3+I2![]() Na2S4O6+2NaI)
Na2S4O6+2NaI)
�����ClO2��Ũ��Ϊ______g/L(�ú���ĸ�Ĵ���ʽ��ʾ������������)��
���𰸡�Բ����ƿ b 1��2 ����Cl2 4H++5ClO2-=Cl+4ClO2��+2H2O 135cV1/V0
��������
����ʵ��װ��ͼ��֪��A��B���Ʊ������Ͷ������ȵģ�C���������������ģ�D���������ն������ȵģ�E�����������ͷŶ������ȵģ�F�ǿ���֤β�����Ƿ���������
(1)����������������֪����A��Բ����ƿ��
(2)Fװ��Ӧ��Cl2��KI��Ӧ������Ҫ����β������װ�ã�����Ӧ���ܽ������̹ܳ�������ѡb��
(3)�����ƺ�ϡ�����ϲ���Cl2��ClO2��NaClO3����Ϊ+5�۱���ԭ��ClO2��+4�ۣ���������Ϊ-1�ۣ���������0���ȣ�ת�Ƶ�����Ϊ2������NaClO3��ClO2ǰ��ѧ������Ϊ2��Cl2ǰ��ѧ������Ϊ1����Ӧ��ѧ����ʽ��2NaClO3+4HCl=2ClO2��+Cl2��+2NaCl+2H2O������������Cl2�ͻ�ԭ����ClO2���ʵ���֮��Ϊ1��2��
(4)Fװ���з���Cl2+2KI=2KCl+I2ʱ���������۱�������F����Һ����ɫ���䣬��װ��C������������Cl2��
(5)������������NaClO2�ɷ�����Ӧ����NaCl���ͷų�ClO2������Ԫ���غ��֪Ӧ����ˮ���ɣ��÷�Ӧ�����ӷ���ʽΪ4H++5ClO2-=Cl+4ClO2��+2H2O��
(6)��ԭClO2��Һ��Ũ��Ϊx mol/L������ݵζ������еķ�Ӧ����ʽ��֪2ClO2��5I2��10Na2S2O3������![]() �����x=
�����x=![]() �����㵥λ��
�����㵥λ��![]() ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���ҹ�ũҵ�������������ɵ���ʧÿ��ߴ�15�ڶ�Ԫ��Ϊ����Ч�������꣬Ŀǰ����Ժ�����ˡ�����������Ͷ���������Ⱦ���������ַ������ȷ��档
(1)������ˮ��Ʒ1�ݣ�ÿ��һ��ʱ��ⶨ����ˮ��Ʒ��pH�����������£�
����ʱ��/h | 0 | 1 | 2 | 3 | 4 |
��ˮ��pH | 4.75 | 4.62 | 4.56 | 4.55 | 4.54 |
�������ݣ��ش��������⣺
����ˮ��Ʒ�����Ե�ԭ����________________________________(�û�ѧ����ʽ��ʾ)��
���������ȡ����������ˮ������ˮ(��������)��ϣ�pH��________(�������������С������������)��
(2)�ⶨ��ˮ��Ʒʱ��ÿ��һ��ʱ��ⶨһ��pH������pH��С����ԭ�������_______(�û�ѧ����ʽ��ʾ)��
(3)��һ��˵��������ˮ���������е�������������ɵ�Ӱ��________________��
����Ŀ������Cu��Fe��Al��Co��Li��Si�ȳɷֵ�ij�Ͻ���ϻ������õĹ���������ͼ��ʾ��

��֪��
��Fe��Co�����ڱ�����ͬ���ڡ�ͬ�壻�����£�pH=7.3ʱLi+��Co3+��ʼ������
���й����ʵ��ܶȻ�(Ksp)��
���� | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
Ksp | 4.0��10-21mol3��L-3 | 1.0��10-32mol4��L-4 | 1.0��10-38mol4��L-4 | 8.0��10-19mol3��L-3 |
�ش���������
��1��Na2CO3��Һ����Ϊ�Ͻ���ϵ����۳����������ӷ���ʽ��ʾ��ԭ��__��
��2�������������е�����Ϊ__��
��3����������Һ������˫��ˮ��������__�������ӷ���ʽ��ʾ����
�ڰ�ˮ�������ǵ�����Һ��pH�������£�ʹ��Һ���������Ӹպó�����ȫ��ȫ����ȥ��Ũ��С��1.0��10-5mol��L-1��Ϊ��ȫ���������������Һ��pH��ΧΪ__��
��4���õ���CoC2O4��2H2O�����ڿ����г�ֱ��տɵ�Co2O3����ѧ����ʽΪ__��
��5����֪Li2CO3����ˮ���䱥����Һ��Ũ�����¶ȵĹ�ϵ�����ʾ��
�¶�/�� | 10 | 30 | 60 |
Ũ��/(mol��L-1) | 0.21 | 0.17 | 0.14 |
�����XΪ����Ũ����__��������__��