题目内容
A、B、C、D、E、F均为短周期元素,且原子序数依次增大,A是原子半径最小的元素,B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4︰1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成离子个数比为2︰1的离子化合物丙。
⑴ D的原子结构示意图为 ,B单质的电子式为 ,E在周期表中的位置为 ;
⑵ 下列说法正确的有 ;
a.化合物乙为正四面体形分子,是由极性键构成的非极性分子
b.C、D、E、F原子半径由大到小的顺序为 C > D > E > F
c.B、E形成的氢化物中,B的氢化物稳定性更强,是因为该分子中存在氢键
d.化合物甲和化合物丙都含有离子键和共价键
⑶ 将F在空气中完全燃烧的产物通入BaCl2和HNO3的混合溶液,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应:
;
⑷ 写出一个由以上元素构成的10 e- 微粒与18 e- 微粒反应的离子方程式:
;
⑸ 在1 mol·L-1 甲溶液中,下列关系式正确的是 ;
a.c(NO3-) > c(NH4+) > c(H+) > c(OH-)
b.c(NH4+) > c(NO3-) > c(H+) > c(OH-)
c.c(NO3-) = c(NH4+) > c(H+) = c(OH-)
d.c(NH4+) = c(NO3-) > c(H+) > c(OH-)
⑹ 25 ℃时,丙的水溶液的pH大于7,其原因是(用离子方程式解释):
。
⑴ 
![]() 第三周期,第ⅤA族
第三周期,第ⅤA族
⑵ a、b
⑶ 3SO2 + 2H2O + 3Ba2+ + 2NO3- === 3BaSO4↓+ 2NO + 4H+
⑷ 2NH3 + H2S === (NH4)2 或者 NH3 + H2S === NH4HS (其它合理答案亦可)
⑸ a
⑹ S2- + H2O ![]() HS- + OH-
HS- + OH-
解析:
略

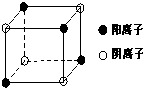 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.