题目内容
【题目】A、B、C、D、E、F六种元素均位于周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子分占四个原子轨道;D元素原子的已成对电子总数是未成对电子总数的3倍;E与D处于同一主族;F位于ds区,且原子的最外层只有1个电子。
(1)F原子的电子排布式是______________。
(2)B、C、D元素的第一电离能由大到小的顺序是(用元素符号表示)__________________。
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B的这种氢化物的化学式是____________;B、C的这些氢化物的沸点相差较大的主要原因是_______________。
(4)A、B、D可形成分子式为A2BD的某化合物,则该化合物分子中B原子的轨道杂化类型是______________;1 mol该分子中含有π键的数目是____________。
(5)写出两种与D3分子互为等电子体的微粒_________。
(6)由A、D、E三种元素组成的两种常见化合物酸性由强到弱为__________,其原因是_________。
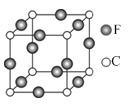
(7)C、F两元素形成的某化合物的晶胞结构如右图所示,则该化合物的化学式是__________________,C原子的配位数是__________________。
【答案】 1s22s22p63s23p63d104s1{或Ar]3d104s1} N>O>C C2H6 氮的氢化物(N2H4)分子间存在氢键 sp2 NA SO2、NO2- H2SO4>H2SO3 二者中H2SO4分子中非羟基氧的个数多,所以H2SO4分子中S的正电性更高,导致S-O-H键中O的电子更向S偏移,更容易电离出H+,故H2SO4的酸性更强些。 Cu3N 6
【解析】A、B、C、D、E、F六种元素均位于周期表的前四周期,且原子序数依次增大;元素A是原子半径最小的元素,则A是H元素;B元素基态原子的核外电子分占四个原子轨道(能级),则B为C元素;D元素原子的已成对电子总数是未成对电子总数的3倍,则D是O元素,C元素原子序数大于B而小于D,则C是N元素;E与D处于同一主族,则E是S元素;F位于ds区,且原子的最外层只有1个电子,则F为Cu元素。
(1)Cu原子核外有29个电子,根据构造原理,铜原子核外电子排布式为1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1;
(2)B、C、D分别是C、N、O元素,且位于同一周期,同一周期元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,所以这三种元素第一电离能大小顺序是N>O>C,故答案为:N>O>C;
(3)C、N元素的某些氢化物的分子中均含有18个电子,则B的这种氢化物为C2H6;含有氢键的氢化物熔沸点较高,氮的氢化物中含有氢键而碳的氢化物中不含氢键,所以氮的氢化物熔沸点较高,故答案为:C2H6;氮的氢化物(N2H4)分子间存在氢键;
(4)H、C、O可形成分子式为H2CO的某化合物,为HCHO,该分子中C原子价层电子对个数是3且不含孤电子对,根据价层电子对互斥理论判断C原子杂化方式为sp2;一个甲醛分子中含有1个π键,则1mol甲醛中含有1molπ键,故答案为:sp2;NA;
(5)与O3分子互为等电子体的微粒有SO2、NO2-,故答案为:SO2、NO2-;
(6)由H、O、S三种元素组成的两种常见化合物为硫酸和亚硫酸,酸性由强到弱的顺序为H2SO4>H2SO3,原因是二者中H2SO4分子中非羟基氧的个数多,所以H2SO4分子中S的正电性更高,导致S-O-H键中O的电子更向S偏移,更容易电离出H+,故H2SO4的酸性更强些,故答案为:H2SO4>H2SO3;二者中H2SO4分子中非羟基氧的个数多,所以H2SO4分子中S的正电性更高,导致S-O-H键中O的电子更向S偏移,更容易电离出H+,故H2SO4的酸性更强些;
(7)N、Cu两元素形成的某化合物的晶胞结构如图所示,该晶胞中Cu原子个数=12×![]() =3、N原子个数=8×
=3、N原子个数=8×![]() =1,所以其化学式为Cu3N;该晶胞中N原子配位数为6,故答案为:Cu3N;6。
=1,所以其化学式为Cu3N;该晶胞中N原子配位数为6,故答案为:Cu3N;6。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案