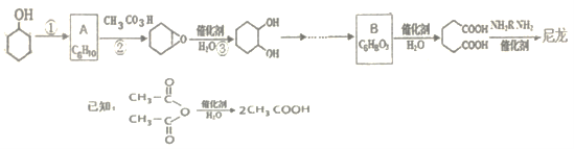
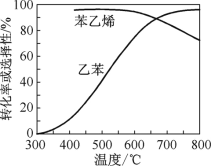
题目内容
【题目】请完成实验室制取蒸馏水的相关内容(装置图见图 1)
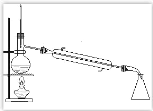
图 1
(1)蒸馏的原理:利用_____不同除去液体混合物中难挥发或不挥发的杂质。
(2)为了避免加热时液体发生暴沸现象,可以在蒸馏烧瓶里加入少量_____。
(3)冷凝管套管下端的开口用橡皮管与自来水龙头相连接,上端开口接上橡皮管后通到水 槽下水道里。即:冷却水从_____进,从_____出。
(4)温度计下端水银球应置于_____处。
【答案】沸点 沸石或碎瓷片 低处 高处 支管口
【解析】
相互混溶的液体混合物或除去液体混合物中难挥发或不挥发的杂质,可根据沸点的差异选择蒸馏操作分离,其操作要点是加入少量沸点防暴沸,冷凝水的水流方向与蒸气的流向相反,温度计的作用是测定蒸气的温度。
(1)蒸馏的原理:利用沸点不同除去液体混合物中难挥发或不挥发的杂质;
(2)为了避免加热时液体发生暴沸现象,可以在蒸馏烧瓶里加入少量沸石或碎瓷片;
(3)为提高冷凝效果,冷水采用逆流而上,则冷却水从低处进,从高处出;
(4)温度计是测定蒸气温度,则温度计下端水银球应置于支管口处。

【题目】一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s) ![]() KCl(l)+NaAlSi3O8(s),完成下列填空:
KCl(l)+NaAlSi3O8(s),完成下列填空:
(1)上述反应涉及的第三周期元素中,离子半径最小的是___;Cl原子与Si原子可构成有5个原子核的分子,其分子的空间构型为____。
(2)用最详尽描述核外电子运动状态的方式,表示氧离子核外电子的运动状态_____。
(3)Na和O2反应形成Na2O和Na2O2的混合物,阴阳离子的个数比为__;NaAlSi3O8改写成氧化物形式是___。
(4)某兴趣小组为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量分数)与温度的关系,进行实验(保持其它条件不变),获得如下数据:
1.5 | 2.5 | 3.0 | 3.5 | 4.0 | |
800℃ | 0.054 | 0.091 | 0.127 | 0.149 | 0.165 |
830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 |
860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 |
950℃ | 0.669 | 0.711 | 0.713 | 0.714 | 0.714 |
分析数据可以得出,氯化钠熔浸钾长石是__________反应(填“放热”或“吸热”);在950℃时,欲提高熔出钾的速率可以采取的一种措施是_______。
(5)Na(l)+KCl(l) ![]() NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,该方法可行的原因是___。
NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,该方法可行的原因是___。
(6)铝可用于冶炼难熔金属,利用铝的亲氧性,还可用于制取耐高温的金属陶瓷。例如将铝粉、石墨和二氧化钛按一定比例混合均匀,涂在金属表面上,然后在高温下煅烧,可在金属表面形成耐高温的涂层TiC,该反应的化学方程式为_____。