��Ŀ����
�ֱ�Ϊ0.6mol��0.5mol��A��B�������壬����0.4L�ܱ������з�����Ӧ��3A��g��+B��g��?mC��g��+2D��g������5min�ﵽƽ�⣬��ʱCΪ0.2mol����֪�ڴ˷�Ӧʱ����D��ƽ����Ӧ����Ϊ0.1mol?L-1?min-1���ش��������⣺
��1��mֵΪ ��
��2��B��ת����Ϊ ��
��3��ƽ��ʱ���������ʵ������ʵ���Ϊ ��
��4�������ֲ�ͬ�������²ⶨ�õ����·�Ӧ���ʣ����б�ʾ�ķ�Ӧ����������
��v��A��=0.5mol?L-1?min-1 ��v��B��=0.2mol?L-1?min-1
��v��C��=0.3mol?L-1?min-1 ��v��D��=0.1mol?L-1?min-1��
��1��mֵΪ
��2��B��ת����Ϊ
��3��ƽ��ʱ���������ʵ������ʵ���Ϊ
��4�������ֲ�ͬ�������²ⶨ�õ����·�Ӧ���ʣ����б�ʾ�ķ�Ӧ����������
��v��A��=0.5mol?L-1?min-1 ��v��B��=0.2mol?L-1?min-1
��v��C��=0.3mol?L-1?min-1 ��v��D��=0.1mol?L-1?min-1��
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
��������1������v=
����v��C������������֮�ȵ��ڻ�ѧ������֮�ȼ���m��
��2�����ݷ���ʽ����μӷ�Ӧ��B�����ʵ�����B��ת����=
��100%��
��3�����ò����������������ܵ����ʵ����仯�����ݴ˼�����
��4�����ݷ�Ӧ����֮�ȵ��ڼ�����֮�ȣ����ͬһ���ʵ����ʣ��ٱȽϴ�С���ɵô𰸣�
| ||
| ��t |
��2�����ݷ���ʽ����μӷ�Ӧ��B�����ʵ�����B��ת����=
| B�����ʵ����仯�� |
| B����ʼ���ʵ��� |
��3�����ò����������������ܵ����ʵ����仯�����ݴ˼�����
��4�����ݷ�Ӧ����֮�ȵ��ڼ�����֮�ȣ����ͬһ���ʵ����ʣ��ٱȽϴ�С���ɵô𰸣�
���
�⣺��1��v��C��=
=0.1mol/��L��min��������֮�ȵ��ڻ�ѧ������֮�ȣ���0.1mol/��L��min����0.1mol/��L��min��=m��2����m=2��
�ʴ�Ϊ��2��
��2�����ݷ���ʽ��֪���μӷ�Ӧ��B�����ʵ���=0.2mol��
=0.1mol����B��ת����=
��100%=20%��
�ʴ�Ϊ��20%��
��3�����ݷ�Ӧ3A��g��+B��g�� ?2C��g��+2D��g������Ӧǰ�������������䣬�ʻ�������ܵ����ʵ������䣬��ƽ��ʱ���������ʵ������ʵ���Ϊ0.6mol+0.5mol=1.1mol��
?2C��g��+2D��g������Ӧǰ�������������䣬�ʻ�������ܵ����ʵ������䣬��ƽ��ʱ���������ʵ������ʵ���Ϊ0.6mol+0.5mol=1.1mol��
�ʴ�Ϊ��1.1mol��
��4������3A��g��+B��g�� ?2C��g��+2D��g������v��A��=0.5mol?L-1?min-1����v��D��=
?2C��g��+2D��g������v��A��=0.5mol?L-1?min-1����v��D��=
v��A��=
��0.1mol?L-1?min-1=0.067mol?L-1?min-1����v��B��=0.2mol?L-1?min-1����v��D��=2v��B��=2��0.2mol?L-1?min-1=0.4mol?L-1?min-1����v��C��=0.3mol?L-1?min-1����v��D��=v��C��=0.3mol?L-1?min-1����v��D��=0.1mol?L-1?min-1���ʢڵķ�Ӧ������ʴ�Ϊ���ڣ�
| ||
| 5min |
�ʴ�Ϊ��2��
��2�����ݷ���ʽ��֪���μӷ�Ӧ��B�����ʵ���=0.2mol��
| 1 |
| 2 |
| 0.1mol |
| 0.5mol |
�ʴ�Ϊ��20%��
��3�����ݷ�Ӧ3A��g��+B��g��
 ?2C��g��+2D��g������Ӧǰ�������������䣬�ʻ�������ܵ����ʵ������䣬��ƽ��ʱ���������ʵ������ʵ���Ϊ0.6mol+0.5mol=1.1mol��
?2C��g��+2D��g������Ӧǰ�������������䣬�ʻ�������ܵ����ʵ������䣬��ƽ��ʱ���������ʵ������ʵ���Ϊ0.6mol+0.5mol=1.1mol���ʴ�Ϊ��1.1mol��
��4������3A��g��+B��g��
 ?2C��g��+2D��g������v��A��=0.5mol?L-1?min-1����v��D��=
?2C��g��+2D��g������v��A��=0.5mol?L-1?min-1����v��D��=| 2 |
| 3 |
| 2 |
| 3 |
���������⿼�黯ѧƽ����йؼ��㣬�ѶȲ���ע������ʹ�ʽ�����������Ӧ�ã�

��ϰ��ϵ�д�
�����Ŀ
��������������Һ���ȣ�������ų����в�����ϡ����İ�ɫ�������ɵ��ǣ�������
| A���������Һ |
| B���������Һ |
| C���������Һ |
| D����������Һ |
�������ӷ���ʽ����д��ȷ���ǣ�������
| A������ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2�� |
| B���ƺ�ˮ��Ӧ��Na+2H2O=Na++2OH-+H2�� |
| C������FeCl3��Һ��Ӧ��Fe+Fe3+�T2Fe2+ |
| D����������Һ�백ˮ��Ӧ��Al3++3NH3?H2O=Al��OH��3��+3NH4+ |
���жԼ�������ʵ������У���ȷ���ǣ�������
| A����������ɫ�������������ܶȶ��Ƚ�С |
| B�������ڿ�����ȼ�����ɵĶ��ǹ������� |
| C�������������ˮ���ҷ�Ӧ���ɼ������ |
| D�����ʵ��ۡ��е�����ԭ�����������Ӷ����� |
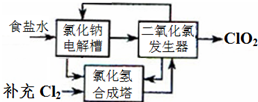 ������������Ƭ����Ч�ɷ֣�ClO2����һ�ָ�Ч����ȫ��ɱ������������
������������Ƭ����Ч�ɷ֣�ClO2����һ�ָ�Ч����ȫ��ɱ������������