题目内容
在某温度下,将H2和I2各0.1mol的气态混合物充入10L的密闭容器中,发生反应H2(g)+I2(g)═2HI(g):充分反映,达到平衡后,测得c(H2)═0.008mol/L,求该反应的平衡常数.( 写计算过程)
考点:化学平衡的计算
专题:化学平衡专题
分析:根据平衡时氢气的浓度,利用三段式计算平衡时碘、HI的浓度,代入平衡常数表达式k=
计算.
| c2(HI) |
| c(I2)?c(H2) |
解答:
解:平衡时,c(H2)=0.008mol?L-1,则:
H2(g)+I2(g) ?2HI(g),
?2HI(g),
开始(mol/L):0.01 0.01 0
变化(mol/L):0.002 0.002 0.004
平衡(mol/L):0.008 0.008 0.004
故平衡常数k=
=
=0.25,
答:该反应的平衡常数为0.25.
H2(g)+I2(g)
 ?2HI(g),
?2HI(g),开始(mol/L):0.01 0.01 0
变化(mol/L):0.002 0.002 0.004
平衡(mol/L):0.008 0.008 0.004
故平衡常数k=
| c2(HI) |
| c(I2)?c(H2) |
| 0.0042 |
| 0.008×0.008 |
答:该反应的平衡常数为0.25.
点评:本题考查化学平衡常数的有关计算,比较基础,注意平衡常数的书写及利用三段式进行的计算.

练习册系列答案
相关题目
下列过程中能引入卤素原子的是( )
| A、在空气中燃烧 | B、取代反应 |
| C、加成反应 | D、加聚反应 |
某高聚物的结构片段如下:
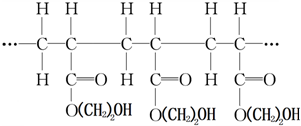
下列分析正确的是( )

下列分析正确的是( )
| A、它是缩聚反应的产物 |
| B、其单体是CH2=CH2COOH和HOCH2CH2OH |
| C、其链节是CH3CH2COO(CH2)2OH |
| D、其单体是CH2=CHCOO(CH2)2OH |
分析确定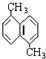 苯环上二氯取代物同分异构体的种数( )
苯环上二氯取代物同分异构体的种数( )
 苯环上二氯取代物同分异构体的种数( )
苯环上二氯取代物同分异构体的种数( )| A、6 | B、8 | C、9 | D、10 |
 在容积固定为2L的密闭容器中,充入0.18molHI,480℃时反应:
在容积固定为2L的密闭容器中,充入0.18molHI,480℃时反应: