��Ŀ����
��4mol SO2��2mol O2����4L���ܱ������У���һ�������·�Ӧ�ﵽƽ�⣺
2SO2��g��+O2��g��?2SO3��g�� ���ƽ��ʱ������ܵ����ʵ���Ϊ5mol�����ڸ������У�ά���¶Ȳ��䣬��a��b��c�ֱ������ʼ�����SO2��O2����SO3�����ʵ�����mol�������a��b��cȡ��ͬ����ֵ�����DZ�������һ�������ϵ�����ܱ�֤�ﵽƽ��ʱ��Ӧ���������������İٷֺ����Ը�����ƽ��ʱ����ȫ��ͬ������д���пհף�
��1�����¶��¸÷�Ӧ��ƽ���� K=
��2��ƽ��ʱSO2��ת����Ϊ
��3����a=0��b=0����c= ��
��4����a=1����b= ��c= ����ʱ��Ӧ�� ���������棩��Ӧ������У�
��5��a��b��c ȡֵ��������һ��������� ��������������ʽ��ʾ��һ��ֻ��a��c����һ��ֻ��b��c����
2SO2��g��+O2��g��?2SO3��g�� ���ƽ��ʱ������ܵ����ʵ���Ϊ5mol�����ڸ������У�ά���¶Ȳ��䣬��a��b��c�ֱ������ʼ�����SO2��O2����SO3�����ʵ�����mol�������a��b��cȡ��ͬ����ֵ�����DZ�������һ�������ϵ�����ܱ�֤�ﵽƽ��ʱ��Ӧ���������������İٷֺ����Ը�����ƽ��ʱ����ȫ��ͬ������д���пհף�
��1�����¶��¸÷�Ӧ��ƽ���� K=
��2��ƽ��ʱSO2��ת����Ϊ
��3����a=0��b=0����c=
��4����a=1����b=
��5��a��b��c ȡֵ��������һ���������
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
���������ݲ������������Ӧ���������ĵĶ����������������ɵ�������������ʵ�����Ȼ������ƽ��ʱ����ֵ�Ũ�ȣ����ݻ�ѧƽ�ⳣ������ʽ��������¶��µ�ƽ�ⳣ��K�����ݵ�Чƽ���˼��ȷ��abc�ķ�Χ���жϷ�Ӧ���еķ���
���
�⣺��Ӧǰ����������ʵ����仯Ϊ����4mol+2mol��-5mol=1mol��
���ݷ�Ӧ�Ļ�ѧ��Ӧ����ʽ��2SO2��g��+O2 ��g�� ?2SO3��g������n
?2SO3��g������n
2 1 2 1
2mol 1mol 2mol 1mol
�ﵽƽ��ʱ����ֵ�Ũ��Ϊ��c��SO2��=
=0.5mol/L��c��O2��=
=0.25mol/L��c��SO3��=
=0.5mol/L��
��1�����¶��µ�ƽ�ⳣ��K=
=
=4���ʴ�Ϊ��4��
��2��ƽ��ʱ���������ת����Ϊ
��100%=50%���ʴ�Ϊ��50%��
��3��2SO2��g��+O2 ��g�� ?2SO3��g��
?2SO3��g��
��ʼ1 4 2 0
��ʼ2 0 0 4
���ݵ�Чƽ��˼�룬�÷�ӦΪǰ��������仯�ķ�Ӧ�����Ա�������ȫ��Ч������c=4���ʴ�Ϊ��4��
��4����a=1ʱ��������ȫ��Ч��˼�룬�൱��4mol��������Ӧ��ȥ��3mol�����ݷ�Ӧ����ʽ���У�
�������������� 2SO2��g��+O2 ��g�� ?2SO3��g��
?2SO3��g��
��ʼ1 4 2 0
��ת������������3������ 1.5 3
��ʼ��1 0.5 3
����b=0.5��c=3
��ʱc��SO2��=0.25mol/L��c��O2��=0.125mol/L��c��SO3��=0.75mol/L��
Qc=
=
=72��K=4������ƽ�����淴Ӧ�����ƶ���
�ʴ�Ϊ��0.5��3���棻
��5��2SO2��g��+O2 ��g�� ?2SO3��g��
?2SO3��g��
��ʼ��mol�� a b c
��ʼ�䣨mol�� a+c b+
c 0
������ȫ��Ч��˼����
���ʴ�Ϊ��
��
���ݷ�Ӧ�Ļ�ѧ��Ӧ����ʽ��2SO2��g��+O2 ��g��
 ?2SO3��g������n
?2SO3��g������n2 1 2 1
2mol 1mol 2mol 1mol
�ﵽƽ��ʱ����ֵ�Ũ��Ϊ��c��SO2��=
| 4mol-2mol |
| 4L |
| 2mol-1mol |
| 4L |
| 2mol |
| 4L |
��1�����¶��µ�ƽ�ⳣ��K=
| c2(SO3) |
| c2(SO2)?c(O2) |
| 0��52 |
| 0��52��0.25 |
��2��ƽ��ʱ���������ת����Ϊ
| 2mol |
| 4mol |
��3��2SO2��g��+O2 ��g��
 ?2SO3��g��
?2SO3��g����ʼ1 4 2 0
��ʼ2 0 0 4
���ݵ�Чƽ��˼�룬�÷�ӦΪǰ��������仯�ķ�Ӧ�����Ա�������ȫ��Ч������c=4���ʴ�Ϊ��4��
��4����a=1ʱ��������ȫ��Ч��˼�룬�൱��4mol��������Ӧ��ȥ��3mol�����ݷ�Ӧ����ʽ���У�
�������������� 2SO2��g��+O2 ��g��
 ?2SO3��g��
?2SO3��g����ʼ1 4 2 0
��ת������������3������ 1.5 3
��ʼ��1 0.5 3
����b=0.5��c=3
��ʱc��SO2��=0.25mol/L��c��O2��=0.125mol/L��c��SO3��=0.75mol/L��
Qc=
| c2(SO3) |
| c2(SO2)?c(O2) |
| 0.752 |
| 0.252��0.125 |
�ʴ�Ϊ��0.5��3���棻
��5��2SO2��g��+O2 ��g��
 ?2SO3��g��
?2SO3��g����ʼ��mol�� a b c
��ʼ�䣨mol�� a+c b+
| 1 |
| 2 |
������ȫ��Ч��˼����
|
|
���������⿼���˻�ѧƽ��ļ��㣬��Ŀ�Ѷ��еȣ�ע���������ò��������м���ķ�������������������ѧ�������������������ѧ��������û���֪ʶ���ʵ���������������ѧ����������

��ϰ��ϵ�д�
�����Ŀ
ij�߾���ĽṹƬ�����£�
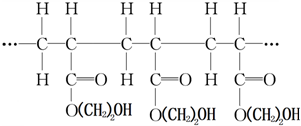
���з�����ȷ���ǣ�������

���з�����ȷ���ǣ�������
| A���������۷�Ӧ�IJ��� |
| B���䵥����CH2=CH2COOH��HOCH2CH2OH |
| C����������CH3CH2COO��CH2��2OH |
| D���䵥����CH2=CHCOO��CH2��2OH |
����ȷ��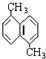 �����϶���ȡ����ͬ���칹���������������
�����϶���ȡ����ͬ���칹���������������
 �����϶���ȡ����ͬ���칹���������������
�����϶���ȡ����ͬ���칹���������������| A��6 | B��8 | C��9 | D��10 |
���з�Ӧ�����ӷ���ʽ��д��ȷ���ǣ�������
| A��FeBr2��Һ��ͨ������Cl2��2Fe2++Cl2�T2Cl-+2Fe3+ |
| B������������Һ��ͨ�����������������壺2ClO-+SO2+H2O�T2HClO+SO32- |
| C��100mL 4mol/L NaOH��Һ��ȫ����6.72L����״���£�CO2��3CO2+4OH-=CO32-+2HCO3-+H2O |
| D����Ũ�ȵ�NH4Al��SO4��2��Һ��Ba��OH��2��Һ��1��2����Ȼ�ϳ��ְ�ɫ������Al3++2SO42-+2Ba2++3OH-=2BaSO4��+Al��OH��3�� |