题目内容
2.有机物A是一种重要的化工原料,在一定条件下可发生如下的转化:
已知:羟基直接连在碳碳双键上的结构(烯醇结构)不稳定,会发生如下重排:

请回答下列问题:
(1)A的结构简式是HC≡CH.
(2)反应①的反应类型是加成反应,写出E的同分异构体CH3OCH3.
(3)F中所含官能团的名称是碳碳双键和羧基.
(4)写出反应④的化学方程式CH3CHO+H2→Ni△→Ni△CH3CH2OH.
(5)写出物质G和NaOH溶液反应的化学方程式CH2=CHCOOCH2CH3+NaOH→CH2=CHCOONa+CH3CH2OH.
分析 B和溴发生加成反应生成C,则B分子式为C8H8,B中不饱和度=8×2+2−828×2+2−82=5,则B中除了含有苯环外还含有一个碳碳双键,则B结构简式为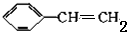 ,则A为HC≡CH,反应①为加成反应;
,则A为HC≡CH,反应①为加成反应;
乙炔和水发生加成反应,根据信息知,D为CH3CHO,D和氢气发生加成反应生成E,E为CH3CH2OH,乙炔和CO、氢气反应生成F,E和F酯化反应生成,则F是酸,分子式为C5H8O2的不饱和度=5×2+2−825×2+2−82=2,说明该物质中还含有一个碳碳双键,根据碳原子守恒知,F结构简式为CH2=CHCOOH,C5H8O2发生加聚反应生成H,G结构简式为CH2=CHCOOCH2CH3,据此分析解答.
解答 解:B和溴发生加成反应生成C,则B分子式为C8H8,B中不饱和度=8×2+2−828×2+2−82=5,则B中除了含有苯环外还含有一个碳碳双键,则B结构简式为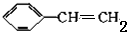 ,则A为HC≡CH,反应①为加成反应;
,则A为HC≡CH,反应①为加成反应;
乙炔和水发生加成反应,根据信息知,D为CH3CHO,D和氢气发生加成反应生成E,E为CH3CH2OH,乙炔和CO、氢气反应生成F,E和F酯化反应生成,则F是酸,分子式为C5H8O2的不饱和度=5×2+2−825×2+2−82=2,说明该物质中还含有一个碳碳双键,根据碳原子守恒知,F结构简式为CH2=CHCOOH,C5H8O2发生加聚反应生成H,G结构简式为CH2=CHCOOCH2CH3,
(1)A的结构简式是HC≡CH,故答案为:HC≡CH;
(2)通过以上分析知,反应①的反应类型是加成反应,E是乙醇,E的同分异构体为CH3OCH3,故答案为:加成反应;CH3OCH3;
(3)F结构简式为CH2=CHCOOH,F中所含官能团的名称是碳碳双键和羧基,故答案为:碳碳双键和羧基;
(4)乙醛被还原生成乙醇,反应④的化学方程式CH3CHO+H2→Ni△→Ni△CH3CH2OH,
故答案为:CH3CHO+H2→Ni△→Ni△CH3CH2OH;
(5)G结构简式为CH2=CHCOOCH2CH3,物质G和NaOH溶液反应生成丙烯酸钠和乙醇,反应方程式为CH2=CHCOOCH2CH3+NaOH→CH2=CHCOONa+CH3CH2OH,故答案为:CH2=CHCOOCH2CH3+NaOH→CH2=CHCOONa+CH3CH2OH.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,根据物质的分子式、反应条件结合题给信息进行推断,知道常见有机物官能团及其性质关系、常见反应类型等知识点,题目难度不大.

 特高级教师点拨系列答案
特高级教师点拨系列答案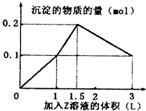 某混合溶液中,含溶质X、Y各0.1mol,向其中滴加0.1mol/L的Z溶液,所得沉淀的物质的量如图,则符合条件的X、Y、Z分别是( )
某混合溶液中,含溶质X、Y各0.1mol,向其中滴加0.1mol/L的Z溶液,所得沉淀的物质的量如图,则符合条件的X、Y、Z分别是( )| A. | 偏铝酸钠、氢氧化钡、硫酸 | B. | 偏铝酸钠、氯化钡、硫酸 | ||
| C. | 氯化铝、氯化镁、氢氧化钠 | D. | 氯化铝、氯化铁、氢氧化钠 |
| A. | 结构片段为 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 | |
| B. | 等质量的乙烯、乙醇、丙烯酸(CH2=CH-COOH)完全燃烧消耗氧气的量相等 | |
| C. | 由甘氨酸、丙氨酸形成的二肽有三种 | |
| D. | 石油的裂化、煤的汽化与液化都属于化学变化,而石油的分馏与煤的干馏都属于物理变化 |
| A. | 强电解质一定易溶于水 | |
| B. | 常温下,强酸和弱酸的浓度相同时,强酸中水的电离程度比弱酸的水的电离程度小 | |
| C. | 对可逆反应,升高温度一定存在v(正)>v(逆) | |
| D. | 钢铁在海水中发生电化腐蚀时,铁是正极被氧化 |
| A. | H2O+2F2═4HF+O2 | B. | H2O+3NO2═2HNO3+NO | ||
| C. | 3H2O+P2O5═2H3PO4 | D. | H2O+Si+2NaOH═2H2↑+Na2SiO3 |

 铜及其化台物在工业、农业、科技和日常生活中有广泛应用.
铜及其化台物在工业、农业、科技和日常生活中有广泛应用.