题目内容
如图表示1~18号元素原子的结构或性质随核电荷数递增的变化。图中纵坐标表示
| A.电子层数 | B.原子半径 | C.最高化合价 | D.最外层电子数 |
D
解析试题分析:电子层数原子序数1-2的相同,原子序数3-10相同,原子序数11-18相同,很显然A选项错误,同周期主族元素,随原子序数递增原子半径减小,B选项错误,第二周期氧、氟两元素没有最高正价,C选项错误,D选项正确。
考点:考查考查元素周期律、结构与性质递变规律。

练习册系列答案
相关题目
下图为元素周期表中短周期的一部分,下列说法错误的是
| X | Y |
| Z | W |
B.单质的活泼性可能是Y<Z
C.X、Z的最高价氧化物对应水化物可能均为强酸
D.分别由Y、W形成的单质可能都是原子晶体
元素的性质呈周期性变化的根本原因是( )
| A.随着元素相对原子质量的递增,量变引起质变 |
| B.元素的原子半径呈周期性变化 |
| C.元素原子核外电子排布呈周期性变化 |
| D.元素的金属性和非金属性呈周期性变化 |
下列表示氮原子结构的化学用语中,对核外电子运动状态描述正确且能据此确定电子的能级的是
A.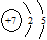 | B.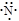 | C.1s22s22p3 | D.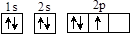 |
离子化合物A2B3是由短周期元素A和B形成,已知A3+离子比B2-离子少一个电子层,以下推断正确的是
| A.化合物A2B3是氧化铝 |
| B.A3+和B2-最外电子层上的电子数都是8 |
| C.A的最高价氧化物对应的水化物是强电解质 |
| D.元素B是第2周期第VIA族的元素 |