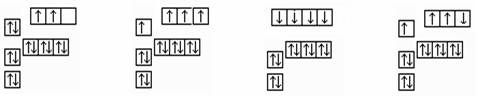
题目内容
短周期主族元素A、B、C、D的原子序数依次增大,A、B、C原子的最外层电子数之和为12,B、C、D位于同一周期,C原子的最外层电子数既是A原子内层电子数的3倍又是B原子最外层电子数的3倍。下列说法正确的是
A.元素A、C的最高价氧化物对应的水化物都是弱酸
B.元素B的单质能与A的最高价氧化物发生置换反应
C.元素B和D能形成BD2型的共价化合物
D.D的氢化物有毒,且有漂白性
B
解析试题分析:由题意知, C原子的最外层电子数既是A原子内层电子数的3倍又是B原子最外层电子数的3倍,则C的最外层电子数为6,B的最外层电子数为2,又 A、B、C原子的最外层电子数之和为12,则A的最外层电子数为4,短周期主族元素A、B、C、D的原子序数依次增大,B、C、D位于同一周期,则A为C元素,B为Mg元素,C为S元素, D为Cl元素;A、A为C元素,对应的最高价氧化物的水化物为碳酸,属于弱酸,C为S元素,对应的最高价氧化物的水化物为硫酸,属于强酸,错误;B、根据反应:2Mg+CO2 2MgO+C,该反应为置换反应,正确;C、B为Mg,D为Cl,二者形成的化合物为离子化合物,错误;D、D为Cl,氯化氢没有漂白性,错误。
2MgO+C,该反应为置换反应,正确;C、B为Mg,D为Cl,二者形成的化合物为离子化合物,错误;D、D为Cl,氯化氢没有漂白性,错误。
考点:考查元素推断及相关物质的结构和性质。

练习册系列答案
相关题目
如图表示1~18号元素原子的结构或性质随核电荷数递增的变化。图中纵坐标表示
| A.电子层数 | B.原子半径 | C.最高化合价 | D.最外层电子数 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH >Ba(OH)2 |
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是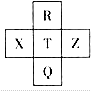
| A.非金属性:Z>T>X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R<T<Q |
| D.R、T、Q的最高正价相同 |
几种短周期元素的原子半径及主要化合价见下表:
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.130 | 0.090 | 0.102 | 0.118 | 0.073 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
根据表中信息,判断以下说法正确的是
A.单质与稀硫酸反应的速率快慢:R>Y>X
B.离子半径:T2->X2+
C.元素最高价氧化物对应水化物的碱性:Y>R>X
D.单质与氢气化合的容易程度:Z>T
原子序数在3~9之间的元素,随着核电荷数的递增而逐渐增大的是
| A.电子层数 | B.最外层电子数 | C.原子半径 | D.化合价 |
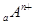 、
、 、
、 、
、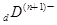 电子层结构相同。关于A、B、C、D四种元素叙述正确的是
电子层结构相同。关于A、B、C、D四种元素叙述正确的是