��Ŀ����
12��ij�о���ѧϰС�����������й�װ�ö�SO2�����ʼ�������SO2�ĺ�������̽����װ�õ��������Ѽ�飩��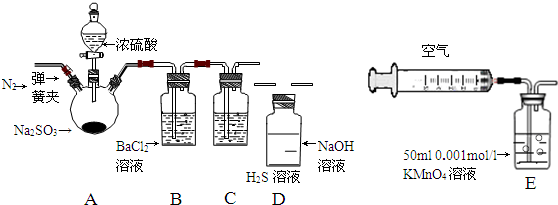
��1��װ��A�з�Ӧ�Ļ�ѧ����ʽ��Na2SO3+H2SO4��Ũ��=Na2SO4+SO2��+H2O��
��2���μ�Ũ����֮ǰ�����ɼУ�ͨ��һ��ʱ��N2���ٹرյ��ɼУ��˲�����Ŀ�����ų�װ����������ʵ��ĸ��ţ�
��3��ʵ�����װ��B��û�����Ա仯��ʵ�����ȡ��װ��B�����зֱ�ȡ������Һ����֧�ྻ�Թ��У����1֧�Թ��еμ�������ˮ���ְ�ɫ����BaSO3���ѧʽ�������2֧�Թ��еμ�����������ˮ����Ȼ���ְ�ɫ�������÷�Ӧ�����ӷ���ʽ��Ba2++SO2+Cl2+2H2O=BaSO4��+4H++2Cl-��
��4��װ��C�е���Һ�г��ֵ���ɫ���ǣ���ʵ��֤��SO2���������ԣ�
��5��װ��D������������SO2β������ֹ��Ⱦ������
��6��ʵ��ⶨװ��D����Һ�ʼ��ԣ���ҺΪʲô�ʼ����أ���������ֲ�ͬ�ļ��裺�������ɵ�Na2SO3ˮ�⣻������������ʣ�࣮�����ʵ�鷽��֤�����ּ������������ѡ�����Լ�����ʵ�飺Na2SO3��Һ����̪��Һ����ˮ��BaCl2��Һ��ϡ����
| ʵ�鲽�� | ʵ����� | Ԥ����������� |
| 1 | ȡ������Һ���Թܣ����뼸�η�̪ | ��Һ��� |
| 2 | Ȼ�����������BaCl2��Һ | ��Һ�в�����ɫ�������������ɫ��ȥ����˵������ȷ������ɫ������ȥ����˵������ȷ |
���� ��1��װ��A���������ƺ�Ũ���ᷴӦ���������ơ��������������ˮ���ݴ�д����Ӧ�Ļ�ѧ����ʽ��
��2��װ��������Ӱ��ⶨ����Ҫ�õ�����ȥ�����еĿ�����
��3����������������ˮ�����Ƕ����������Ȼ�����Һ��Ӧ��������Һ��ͨ�백��������������泥����������Һ���Ȼ�����Ӧ���������ᱵ����������ǿ�����ԣ������������������������ᣬ�������Ȼ�����Ӧ�����Ȼ����������ݴ�д����Ӧ�����ӷ���ʽ��
��4���������������ⷴӦ���ɵ���ɫ��S���ʣ�������������������ԣ�
��5�����������ж��������������Ҫ������������Һ���գ�
��6����ʵ��1����Һ�м��������Ȼ�����Һ��������Һ��ɫ�仯�жϣ�
��7�����ݻ��ϼ۱仯�ҳ����������������صķ�Ӧ��ϵʽ��Ȼ����ݸ�����ص����ʵ��������VmL�����к��еĶ�������������Ȼ�����������ж�����������������
��� �⣺��1��װ��A���������ƺ�Ũ���ᷴӦ���ɶ����������壬��Ӧ�Ļ�ѧ����ʽΪ��Na2SO3+H2SO4��Ũ��=Na2SO4+SO2��+H2O��
�ʴ�Ϊ��Na2SO3+H2SO4��Ũ��=Na2SO4+SO2��+H2O��
��2��װ���е�����Ӱ������������IJⶨ������Ϊ���ų�װ���п�����Ӧ�õμ�Ũ����֮ǰ�����ɼУ�ͨ��һ��ʱ��N2���ٹرյ��ɼУ�
�ʴ�Ϊ���ų�װ����������ʵ��ĸ��ţ�
��3�����1֧�Թ��еμ�������ˮ����ˮ���������Ӧ����������泥�����������Ȼ�����Ӧ���������ᱵ��ɫ�����������������������������ᣬ�����뱵���ӷ�Ӧ�������ᱵ��������Ӧ�����ӷ���ʽΪ��Ba2++SO2+Cl2+2H2O=BaSO4��+4H++2Cl-��
�ʴ�Ϊ��BaSO3��Ba2++SO2+Cl2+2H2O=BaSO4��+4H++2Cl-��
��4��C�з�����ӦΪ��2H2S+SO2=3S��+2H2O����Ӧ�ж�������õ��ӻ��ϼ۽��Ͷ����������������������ԣ�
�ʴ�Ϊ��������
��5����������������һ���ж����������������������岻��ֱ���ŷţ���Ҫ������������Һ���գ�
�ʴ�Ϊ������SO2β������ֹ��Ⱦ������
��6��ȡ������Һ���Թܣ����뼸�η�̪����Һ��ɺ�ɫ��Ȼ�������Һ��Ȼ�����������BaCl2��Һ����Һ�в�����ɫ������������ɫ��ȥ����˵������ȷ������ɫ������ȥ����˵������ȷ��
| ʵ�鲽�� | ʵ����� | Ԥ����������� |
| 2 | Ȼ�����������BaCl2��Һ | ��Һ�в�����ɫ�������������ɫ��ȥ����˵������ȷ������ɫ������ȥ����˵������ȷ |
��ÿ�����SO2���������Ϊ��$\frac{2.8mL}{VmL}$=$\frac{2.8}{V}$��
�ʴ�Ϊ��$\frac{2.8}{V}$��
���� ���⿼����̽���������ʡ��������ʺ����ķ�������Ŀ�ѶȽϴ�����֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ�����ѧ���ķ�����������������ȷʵ��ԭ������ѧʵ�������������Ϊ���ؼ�����6��Ϊ�״��㣬ע������ʵ�鷽�������������ԭ��

 �Ķ��쳵ϵ�д�
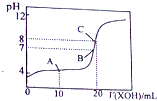
�Ķ��쳵ϵ�д�| A�� | Һ���ڡ�0���̶�ʱ��50 mL��ʽ�ζ��ܺ�25 mL��ʽ�ζ�����ʢҺ�����������ֵһ��Ϊ2��1 | |
| B�� | ��NaOH��Һ�Ͱ�ˮ��Һ��ϡ��һ�������ߵ�OH-Ũ�Ⱦ����ٵ�ԭ���Ķ���֮һ | |
| C�� | ��������Ũ���Ǵ���Ũ�ȵĶ������������H+Ũ��Ҳ�Ǵ���Ķ��� | |
| D�� | ��ȡTiO2����TiCl4�Ӵ���ˮ��ͬʱ���ȣ�TiCl4+��x+2��H2O��������?TiO2•xH2O��+4HCl�����õ�TiO2•H2O�����յ�TiO2 |
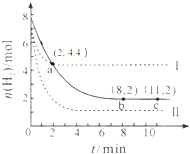 ij�¶��£���6mol CO2��8mol H2 ����2L�ܱ������з�����ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g����H��0��������H2�����ʵ�����ʱ��ı仯��ϵ����ͼ�е�ʵ����ʾ��ͼ�����߱�ʾ���ı�ijһ��Ӧ����ʱ��H2�����ʵ�����ʱ��ı仯��ϵ������˵����ȷ���ǣ�������
ij�¶��£���6mol CO2��8mol H2 ����2L�ܱ������з�����ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g����H��0��������H2�����ʵ�����ʱ��ı仯��ϵ����ͼ�е�ʵ����ʾ��ͼ�����߱�ʾ���ı�ijһ��Ӧ����ʱ��H2�����ʵ�����ʱ��ı仯��ϵ������˵����ȷ���ǣ�������| A�� | ���ߢ��Ӧ�������ı���ܽ����¶� | |
| B�� | ���ߢ��Ӧ�������ı�����dz��뺤�� | |
| C�� | ���¶��£��˷�Ӧ�Ļ�ѧƽ�ⳣ������ֵΪ0.5 | |
| D�� | �ӷ�Ӧ��ʼ��a �㣬�ͣ�CO2��=0.6 mol•L-1•min-1 |
| A�� | CH3CH��CH3��2������״������ | B�� | 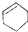 ���ڷ����廯���� ���ڷ����廯���� | ||
| C�� | 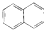 ����֬�������� ����֬�������� | D�� | 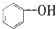 ���ڷ����� ���ڷ����� |
| A�� | ͬһ�����еĵڢ�A��͵ڢ�A��Ԫ�ص�ԭ��������һ��Ϊ1 | |
| B�� | L���ϵĵ�����Ϊ������Ԫ��һ��������Ԫ�� | |
| C�� | ͬһ���������������ڵ�Ԫ�ص�ԭ��������Ϊ��һ��������Ԫ������ | |
| D�� | ��������������������Ԫ��һ���ǽ���Ԫ�� |
��2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
��2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2��
����˵����ȷ���ǣ�������
| A�� | ������Ӧ�о�Ϊ��Ԫ�ر����� | |
| B�� | ��Ӧ�١��������ɵ�����I2ʱת�Ƶ�������Ϊ1��5 | |
| C�� | �����ԣ�MnO2��SO42-��IO3-��I2 | |
| D�� | ��Ԫ���ڷ�Ӧ���б���ԭ���ڷ�Ӧ���б����� |
 X��Y��Ԫ�����ڱ�ǰ20��Ԫ�أ���X��ԭ��������Y��4������գ�X��YҪ�þ����Ԫ�ط��ű�ʾ����
X��Y��Ԫ�����ڱ�ǰ20��Ԫ�أ���X��ԭ��������Y��4������գ�X��YҪ�þ����Ԫ�ط��ű�ʾ����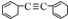 �IJ����Ͷ�Ϊ��������
�IJ����Ͷ�Ϊ��������