题目内容
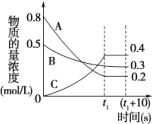
【题目】将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g)。2min后,测得D的浓度为
xC(g)+2D(g)。2min后,测得D的浓度为![]() mol/L ,
mol/L ,![]() ,C的反应速率是
,C的反应速率是![]() mol/(L·min)。则:
mol/(L·min)。则:
①x的值是__________;
②B的平均反应速率是____________;
③A在2min末的浓度是________________。
【答案】2 0.125mol/(L·min) 0.75mol/L
【解析】
由C的反应速率是![]() mol/(L·min)可知,2min末C的浓度为
mol/(L·min)可知,2min末C的浓度为![]() mol/(L·min) ×2min=0.5mol/L,设起始A和B的物质的量为amol/L,由题给数据建立如下三段式:
mol/(L·min) ×2min=0.5mol/L,设起始A和B的物质的量为amol/L,由题给数据建立如下三段式:
3A(g)+B(g) ![]() xC(g)+2D(g)
xC(g)+2D(g)
起(mol/L) a a 0 0
变(mol/L) 0.75 0.25 0.5 0.5
平(mol/L) a—0.75 a—0.25 0.5 0.5
①由三段式可知,C和D的浓度变化量之比为0.5mol/L:0.5mol/L=1:1,因物质的变化量之比等于化学计量数之比,则x:2=1:1,解得x=2,故答案为:2;
②由三段式可知,B的浓度变化量△c(B)=![]() =
=![]() = 0.125mol/(L·min),故答案为:0.125mol/(L·min);
= 0.125mol/(L·min),故答案为:0.125mol/(L·min);
③由2min末c(A):c(B)=3:5可得关系式:(a—0.75):(a—0.25)=3:5,解得a=1.5,则A在2min末的浓度为(1.5—0.75)mol/L=0.75 mol/L,故答案为:0.75 mol/L。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目