题目内容
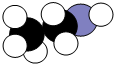 如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质说法不正确为( )
如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质说法不正确为( )| A、不能使紫色石蕊变红 |
| B、与碳酸钠反应 |
| C、能发生酯化反应 |
| D、能发生氧化反应催化剂 |
考点:乙醇的化学性质
专题:有机物的化学性质及推断
分析:比例模型可以直观地表示分子的形状,其碳原子的成键情况是确定分子结构的关键,碳原子的成键情况主要根据与碳原子形成共价键的原子的数目确定,原子半径的关系为C>O>H,依此进行判断.
解答:
解:由比例模型可以看出分子中有2个碳原子和1个氧原子,6个氢原子,则结构简式为CH3CH2OH.
A.CH3CH2OH不能电离出氢离子,不能使紫色石蕊变红,故A正确;
B.CH3CH2OH与碳酸钠不反应,故B错误;
C.CH3CH2OH能与CH3COOH发生酯化反应,故C正确;
D.CH3CH2OH能发生催化氧化生成乙醛,故D正确,
故选B.
A.CH3CH2OH不能电离出氢离子,不能使紫色石蕊变红,故A正确;
B.CH3CH2OH与碳酸钠不反应,故B错误;
C.CH3CH2OH能与CH3COOH发生酯化反应,故C正确;
D.CH3CH2OH能发生催化氧化生成乙醛,故D正确,
故选B.
点评:本题考查学生利用比例模型来分析CH3CH2OH分子,难度不大,明确模型中碳、氢、氧原子的大小及个数是解答本题的关键.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
化学中常用图象直观地描述化学反应的进程或结果,下列图象描述正确的是( )
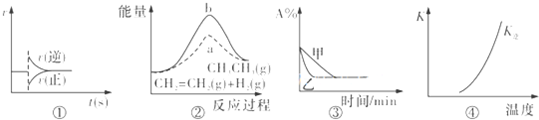

| A、图①可以表示某化学平衡体系改变温度后,反应速率随时间的变化 |
| B、图②中a、b曲线分别表示反应CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0未使用和使用催化剂时,反应过程中的能量变化 |
| C、图③表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(g)影响,且甲的压强大 |
| D、图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0反应的平衡常数K随温度的变化 |
下列氧化还原反应中,电子得失情况表示不正确的是( )
A、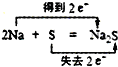 |
B、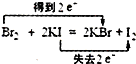 |
C、 |
D、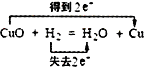 |
下面有关Na2CO3与NaHCO3的性质比较中错误的是( )
| A、相同浓度溶液的碱性:Na2CO3>NaHCO3 |
| B、同温下在水中的溶解度:Na2CO3>NaHCO3 |
| C、滴加同浓度的硫酸,反应先放出气泡的是Na2CO3 |
| D、热稳定性:NaHCO3<Na2CO3 |
下列有关有机物同分异构体说法中不正确的是( )
| A、分子式为C4H8的同分异构体共有(不考虑立体异构)5种 |
| B、立方烷(C8H8)的六氯取代物有3种 |
| C、分子式为C5H12O的同分异构体中属于醇类的有7种 |
D、 的一溴取代物有4种 的一溴取代物有4种 |
下列反应中亚硫酸溶液表现的性质与另外三种不同的是( )
| A、能使酸性高锰酸钾溶液褪色 |
| B、在空气中久置,溶液pH变小 |
| C、能使溴水褪色 |
| D、加入氢氧化钡溶液产生白色沉淀 |
已知:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O,2FeCl2+Cl2=2FeCl3,下列物质的氧化性由强到弱的顺序是( )
| A、KMnO4>Cl2>FeCl3 |
| B、Cl2>KMnO4>FeCl3 |
| C、FeCl3>Cl2>KMnO4 |
| D、FeCl3>KMnO4>Cl2 |
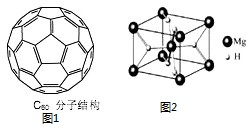 氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.
氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.