题目内容
17.在下列条件下,两瓶气体所含的原子数一定相等的是( )| A. | 具有同质量、不同体积的N2O和CO2 | B. | 具有同温度、同体积的CO和N2 | ||
| C. | 具有同体积、同密度的SO2和NO2 | D. | 具有同密度、不同质量的O2和O3 |
分析 A.二者的摩尔质量相等,同质量时,物质的量相同,分子数相同,原子数相同;
B.同温度、同体积,气体分子数目与压强呈正比;
C.同体积、同密度的SO2和NO2质量相等,二者摩尔质量不相等,二者物质的量不等;
D.O2和O3都由氧原子构成,O2和O3质量不相等,则含有的氧原子数目不相等.
解答 解:A.N2O和CO2的摩尔质量都为44g/mol,根据n=$\frac{m}{M}$可知:同质量时,物质的量相同,分子数相同,1分子N2O和1分子CO2的原子数相同,所以具有同质量、不同体积的N2O和CO2所含的原子数一定相等,故A正确;
B.同温度、同体积,气体分子数目与压强呈正比,压强不定,无法判断气体分子数关系,故B错误;
C.根据m=ρv可知同体积、同密度的SO2和NO2质量相等,根据n=$\frac{m}{M}$可知:二者物质的量之比为46:64=23:32,每个分子都含有3个原子,所以含有原子数目之比为69:96,故C错误;
D.O2和O3都由氧原子构成,氧原子质量相等,O2和O3质量不相等,则含有的氧原子数目不相等,故D错误;
故选A.
点评 本题考查物质的量的有关计算,掌握阿伏伽德罗定律及推论以及物质的量与体积、质量之间相互转化公式的熟练运用是解答关键,题目难度不大.

练习册系列答案
相关题目
7.根据下列四种粒子的结构示意图,所获取的信息不正确的是( )
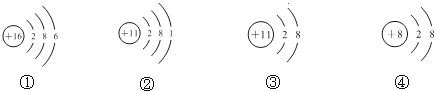
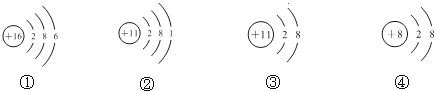
| A. | 它们表示三种元素 | |
| B. | ②③的化学性质相同 | |
| C. | ②表示的元素是金属元素 | |
| D. | ①表示的是原子,而④表示的是阴离子 |
8.下列电子式中,正确的是( )
| A. | 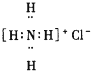 | B. | 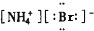 | C. | 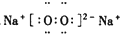 | D. | 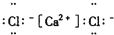 |
9.X和Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,已知X的原子序数比Y的原子序数大,下列说法中正确的是( )
| A. | X的金属性比Y的金属性强 | |
| B. | 常温下,X和Y都不能从水中置换出氢 | |
| C. | Y元素的氢氧化物碱性比X元素的氢氧化物碱性大 | |
| D. | X元素的最高化合价比Y元素的最高化合价低 |
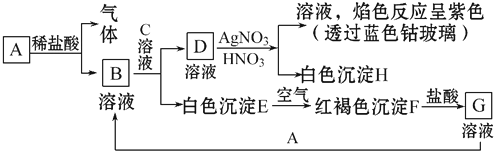

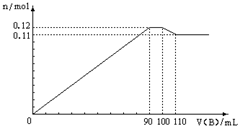 向100mLBaCl2、AlCl3、FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀和加入混合溶液B的体积关系如下图所示:
向100mLBaCl2、AlCl3、FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀和加入混合溶液B的体积关系如下图所示: