题目内容
7.根据下列四种粒子的结构示意图,所获取的信息不正确的是( )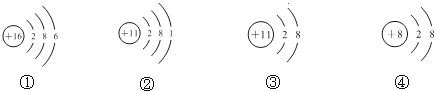
| A. | 它们表示三种元素 | |
| B. | ②③的化学性质相同 | |
| C. | ②表示的元素是金属元素 | |
| D. | ①表示的是原子,而④表示的是阴离子 |
分析 元素的概念为:具有相同质子数的一类原子的总称,所以不同种元素最本质的区别是质子数不同;①是S元素,②、③表示的是同一种元素是钠元素,钠元素为金属元素;④是O元素,据此对各选项进行判断.
解答 解:A.具有相同质子数的一类原子的总称,所以同种元素必须具有相同的质子数,①为S元素,②、③表示的是钠元素,④为O元素,总共有三种元素,故A正确;
B.②为钠原子,具有较强的还原性,③为钠离子,化学性质比较稳定,所以二者的化学性质区别较大,故B错误;
C.②为钠原子,钠元素属于金属元素,故C正确;
D.①中的核电荷数=核外电子总数,所以表示的是S原子,④中核电荷数<核外电子总数,所以表示的是阴离子,故D正确;
故选B.
点评 本题考查了粒子结构示意图的表示方法,题目难度不大,注意明确离子结构示意图与原子结构示意图的表示方法,明确同种的原子与阴阳离子的化学性质的区别.

练习册系列答案
相关题目
18.将下列浓溶液蒸干并灼烧,可以得到原溶质的是( )
| A. | 氯化钠 | B. | 碳酸氢钠 | C. | 偏铝酸钠 | D. | 氯化铁 |
15.现有X、Y两种原子,X原子的M层比Y原子的M层少3个电子,Y原子L层的电子数为X原子L层电子数的2倍,则X和Y分别是( )
| A. | 硅原子和钠原子 | B. | 硼原子和氦原子 | C. | 氯原子和碳原子 | D. | 碳原子和铝原子 |
2.根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价] | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | L2+与R2-的核外电子数相等 | D. | M与T形成的化合物具有两性 |
16.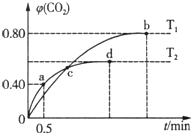 利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4mol CO,测得CO2的体积分数随时间t变化曲线如图.下列说法不正确的是( )
利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4mol CO,测得CO2的体积分数随时间t变化曲线如图.下列说法不正确的是( )
 利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4mol CO,测得CO2的体积分数随时间t变化曲线如图.下列说法不正确的是( )
利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4mol CO,测得CO2的体积分数随时间t变化曲线如图.下列说法不正确的是( )| A. | T2时,0~0.5 min内的反应速率v(CO)=1.6mol/(L•min) | |
| B. | 两种温度下,c点时体系中混合气体的压强相等 | |
| C. | d点时,增大体系压强,CO的转化率不变 | |
| D. | b点和d点时化学平衡常数的大小关系:Kb>Kd |
17.在下列条件下,两瓶气体所含的原子数一定相等的是( )
| A. | 具有同质量、不同体积的N2O和CO2 | B. | 具有同温度、同体积的CO和N2 | ||
| C. | 具有同体积、同密度的SO2和NO2 | D. | 具有同密度、不同质量的O2和O3 |
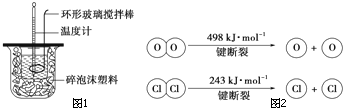 针对化学反应中的能量变化解决下列问题.
针对化学反应中的能量变化解决下列问题.
 .
. .
. 2,3,4,5-四甲基己烷
2,3,4,5-四甲基己烷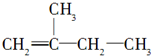 2-甲基-1丁烯
2-甲基-1丁烯 .
. .
. 分子式为C10H20,按碳的骨架分,该有机物属于ab.(填字母序号)
分子式为C10H20,按碳的骨架分,该有机物属于ab.(填字母序号)