题目内容
17.已知物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关.下列各组物质:①Cu与HNO3溶液②Al与NaOH溶液③Zn与H2SO4溶液④Mg与HCl溶液.由于浓度不同而能发生不同氧化还原反应的是( )| A. | ③④ | B. | ①③ | C. | ①② | D. | ①③④ |
分析 ①Cu与HNO3溶液反应,如果是浓硝酸,二者反应生成二氧化氮,如果是稀硝酸,二者反应生成NO;
②Al与NaOH溶液反应,无论NaOH溶液是浓溶液还是稀溶液都生成偏铝酸钠和氢气;
③Zn与H2SO4溶液反应,如果是浓硫酸,二者反应生成二氧化硫,如果是稀溶液,二者反应生成氢气;
④Mg与HCl溶液反应,无论是浓盐酸还是稀盐酸都生成氢气和氯化镁.
解答 解:①Cu与HNO3溶液反应,如果是浓硝酸,二者反应生成二氧化氮,如果是稀硝酸,二者反应生成NO,所以产物与溶液浓度有关,故选;
②Al与NaOH溶液反应,无论NaOH溶液是浓溶液还是稀溶液都生成偏铝酸钠和氢气,所以产物与溶液浓度无关,故不选;
③Zn与H2SO4溶液反应,如果是浓硫酸,二者反应生成二氧化硫,如果是稀溶液,二者反应生成氢气,所以产物与溶液浓度有关,故选;
④Mg与HCl溶液反应,无论是浓盐酸还是稀盐酸都生成氢气和氯化镁,所以产物与溶液浓度无关,故不选;
故选B.
点评 本题考查物质之间反应,为高频考点,明确物质性质是解本题关键,影响产物的因素有反应物浓度、反应物用量、反应温度等,题目难度不大.

练习册系列答案
相关题目
7.氢气是21世纪最理想的能源,其根据不正确的是( )
| A. | 生产氢气的原料来源广泛 | |
| B. | 氢气燃烧时无污染 | |
| C. | 氢气易液化,贮存、携带方便 | |
| D. | 在等质量的可燃气体中,氢气燃烧时放出的热量多 |
8.下列离子方程式正确的是( )
| A. | 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 铁与盐酸的反应 Fe+2H+═Fe3++H2↑ | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 纯碱和稀盐酸反应 CO32-+2H+═CO2↑+H2O |
6.人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化、聚乙烯、二氧化硅等17种“分子”改变过人类的世界.
(1)铁原子在基态时,价电子(外围电子)排布式为3d64s2.
(2)硝酸钾中NO3-的空间构型为平面正三角形,写出与NO3-互为等电子体的一种非极性分子化学式BF3[SO3( g)、BBr3等].
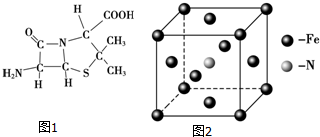
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有C、N、O、S.
(4)下列说法正确的有a(填字母序号).
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(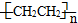 )分子中有5n个σ键
)分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
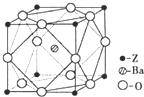
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图2所示,写出该反应的化学方程式8Fe+2NH3$\frac{\underline{\;640℃\;}}{\;}$2Fe4N+3H2.若两个最近的Fe原子间的距离为s cm,则该晶体的密度是$\frac{{119\sqrt{2}}}{{2{s^3}{N_A}}}$g•mol-1.
(1)铁原子在基态时,价电子(外围电子)排布式为3d64s2.
(2)硝酸钾中NO3-的空间构型为平面正三角形,写出与NO3-互为等电子体的一种非极性分子化学式BF3[SO3( g)、BBr3等].
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有C、N、O、S.

(4)下列说法正确的有a(填字母序号).
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(
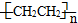 )分子中有5n个σ键
)分子中有5n个σ键d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
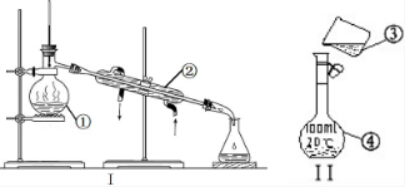 掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实
 Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素.已知:
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素.已知: