题目内容
3.A~J分表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素.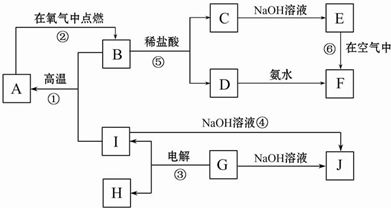
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在周期表中的位置第四周期第Ⅷ族.
(2)写出反应①、⑤、⑥的化学方程式和反应④的离子方程式.
反应①:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe
反应⑤:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
反应⑥:4Fe(OH)2+O2+2H2O4═Fe(OH)3
反应④:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(3)从能量变化的角度看,①、②、③反应中,△H<0的是①②(填序号).
分析 G为主族元素的固态氧化物,电解G得到I和H,G能和氢氧化钠溶液反应生成J,工业上用电解氧化铝的方法冶炼铝,则G是Al2O3,I能和氢氧化钠溶液反应生成J,则I是Al,J是NaAlO2,H是O2,Al和B能在高温下反应生成A,A能在氧气中燃烧生成B,铝在高温下能发生铝热反应,则B是金属氧化物,A是金属单质,B和盐酸反应生成C和D,C和氢氧化钠反应生成E,D和氨水反应生成F,E在空气中反应生成F,说明E不稳定,易被氧气氧化,且A、B、C、D、E、F六种物质中均含同一种元素,则A是Fe,B为Fe3O4,C为FeCl2,D为FeCl3,E为Fe(OH)2,F为Fe(OH)3,结合对应单质、化合物的性质解答该题.
解答 解:G为主族元素的固态氧化物,电解G得到I和H,G能和氢氧化钠溶液反应生成J,工业上用电解氧化铝的方法冶炼铝,则G是Al2O3,I能和氢氧化钠溶液反应生成J,则I是Al,J是NaAlO2,H是O2,Al和B能在高温下反应生成A,A能在氧气中燃烧生成B,铝在高温下能发生铝热反应,则B是金属氧化物,A是金属单质,B和盐酸反应生成C和D,C和氢氧化钠反应生成E,D和氨水反应生成F,E在空气中反应生成F,说明E不稳定,易被氧气氧化,且A、B、C、D、E、F六种物质中均含同一种元素,则A是Fe,B为Fe3O4,C为FeCl2,D为FeCl3,E为Fe(OH)2,F为Fe(OH)3,
(1)A、B、C、D、E、F六种物质中所含的同一种元素是Fe元素,铁元素位于第四周期第Ⅷ族,
故答案为:第四周期第Ⅷ族;
(2)反应①为高温下铝和四氧化三铁反应生成氧化铝和铁,反应的化学方程式为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe;
反应⑤为四氧化三铁与稀盐酸反应生成氯化亚铁、氯化铁和水,反应的化学方程式为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;
反应⑥为氢氧化亚铁不稳定易被氧气氧化生成氢氧化铁,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
反应④为铝和氢氧化钠反应生成偏铝酸钠和氢气,反应的离子反应方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe;Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;4Fe(OH)2+O2+2H2O4═Fe(OH)3;2Al+2OH-+2H2O═2AlO2-+3H2↑;
(3)△H<O的反应为放热反应,①为铝热反应,②为燃烧反应,均为常见的放热反应,③为电解反应,为吸热反应,
故答案为:①②.
点评 本题考查无机物的推断,题目难度中等,注意根据物质的性质和典型反应现象进行推断,熟练掌握元素化合物性质为解答关键,试题培养了学生的逻辑推理能力及灵活应用能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 当Al3+恰好完全沉淀时,消耗Ba(OH)2 1.5 mol | |
| B. | 当SO42-恰好完全沉淀时,Al3+全部转化为AlO2- | |
| C. | 当向溶液中加入1.5 mol Ba(OH)2时,反应可用下列离子方程式表示:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 随着加入的Ba(OH)2的物质的量不断增大,沉淀的物质的量不断增大 |
(1)配制250mL0.1mol/L的盐酸溶液
| 应量取该浓盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
A、用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B、用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C、将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶,溶液注入容量瓶前需恢复到室温,这是因为容量瓶盛放热溶液时,体积不准;
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作偏低;若加蒸馏水时不慎超过了刻度线偏低;若定容时俯视刻度线偏高.
(5)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度线重新配制;向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面重新配制.
| A. | 在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 | |
| B. | 1 mol羟基中电子数为10NA | |
| C. | 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g | |
| D. | 常温下,1 L 0.1 mol•L-1的NH4NO3溶液中氮原子数为0.2NA |
| A. | 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 铁与盐酸的反应 Fe+2H+═Fe3++H2↑ | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 纯碱和稀盐酸反应 CO32-+2H+═CO2↑+H2O |
①FeCl2 ②FeCl3 ③Fe(OH)3 ④HCl.
| A. | 只有①②③ | B. | 只有②③ | C. | 只有①③④ | D. | 全部 |