题目内容
20.对金属制品进行抗腐蚀处理,可延长其使用寿命.(1)利用如图装置,可以模拟铁的电化学防护.
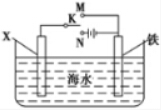
若X为碳棒,为减缓铁的腐蚀,开关K应置于N处.若X为锌,开关K置于M处,该电化学防护法称为牺牲阳极保护法(或牺牲阳极的阴极保护法).
(2)以下为铝材表面处理的一种方法:
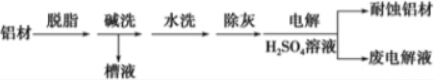
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是2Al+2OH-+2H2O═2AlO+3H2↑ (用离子方程式表示).
为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的b.
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
2Al+3H2O-6e-═Al2O3+6H+.
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是
HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀.
(3)镀铜可防止铁制品腐蚀,电镀时阳极材料为纯铜,用铜而不用石墨作阳极的原因是补充溶液中消耗的Cu2+,保持溶液中Cu2+浓度恒定.
分析 (1)根据金属的防护,若K置于N处,必须让被保护的金属接电源负极;若开关K置于M处,形成原电池,锌作负极,为牺牲阳极保护法(或牺牲阳极的阴极保护法);
(2)①有气泡冒出因2Al+2OH-+2H2O═2AlO2-+3H2↑;因碱洗槽液中有AlO2-,故应通入CO2来回收Al(OH)3,发生反应2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32-或
CO2+2H2O+AlO2-═HCO3-+Al(OH)3↓;若加HNO3,生成的沉淀还会继续溶解;
②铝为阳极,会发生氧化反应,表面形成氧化膜,必须有水参加,所以电极反应式为:2Al+3H2O-6e-═Al2O3+6H+;HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀;
(3)用纯铜作电极可及时补充电镀液中消耗的Cu2+,保持其浓度恒定.
解答 解:(1)金属的防护有牺牲阳极保法和外加电源阴极保护法,若K置于N处,必须让被保护的金属接电源负极;若开关K置于M处,形成原电池,锌作负极,为牺牲阳极保护法(或牺牲阳极的阴极保护法),
故答案为:N;牺牲阳极保护法(或牺牲阳极的阴极保护法);
(2)①铝能与强碱反应产生氢气,Al(OH)3具有两性,既能与强碱反应也能与强酸反应生成盐和水,碱洗槽液中有AlO2-,故应通入CO2来回收Al(OH)3,发生反应2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32-或CO2+2H2O+AlO2-═HCO3-+Al(OH)3↓;若加HNO3,生成的沉淀还会继续溶解,
故答案为:2Al+2OH-+2H2O═2AlO+3H2↑;b;
②铝为阳极,会发生氧化反应,表面形成氧化膜,必须有水参加,所以电极反应式为:2Al+3H2O-6e-═Al2O3+6H+;加入NaHCO3溶液后产生气泡和白色沉淀,是由于废电解液中含有Al3+,和HCO3-发生了互促水解.或HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀,
故答案为:2Al+3H2O-6e-═Al2O3+6H+;HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀;
(3)电镀铜时用纯铜做阳极,阳极上铜被氧化,电解质溶液浓度不变,用铜作电极可及时补充电镀液中消耗的Cu2+,保持其浓度恒定,采用石墨无法补充Cu2+,
故答案为:纯铜;阳极Cu可以发生氧化反应生成Cu2+,补充溶液中消耗的Cu2+,保持溶液中Cu2+的浓度恒定.
点评 本题考查了原电池工作原理、电解原理的综合应用,题目难度中等,明确实验目的及实验原理为解答关键,注意熟练掌握原电池、电解池工作原理,试题培养了学生的分析能力及灵活应用能力.

| A. | x=0.5,a=10 | B. | x=1,a=5 | C. | x=2,a=10 | D. | x=0.5,a=8 |
| A. | 在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 | |
| B. | 1 mol羟基中电子数为10NA | |
| C. | 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g | |
| D. | 常温下,1 L 0.1 mol•L-1的NH4NO3溶液中氮原子数为0.2NA |
| A. | 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 铁与盐酸的反应 Fe+2H+═Fe3++H2↑ | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 纯碱和稀盐酸反应 CO32-+2H+═CO2↑+H2O |
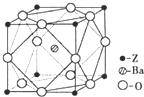 Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素.已知:
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素.已知: