题目内容
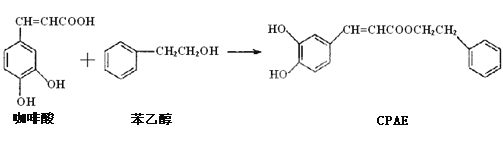
【题目】托特罗定(G)是毒蕈碱受体拮抗剂,其一种合成路线流程图如下:
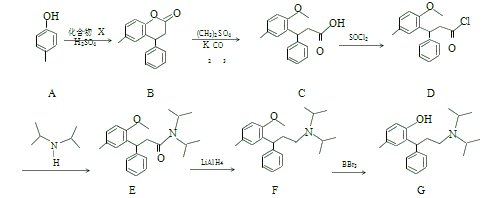
请按要求回答下列问题:
(1)A 的名称:_____;最多共平面的原子数目为_____。C 中含氧官能团名称为_________。
(2)D→E的反应类型为_____。
(3)B 与 NaOH 溶液加热条件下反应的化学方程式:____________。
(4)C→D 反应过程使用的液态 SOCl2(![]() )沸点为 77℃,遇水剧烈反应,产生酸雾和刺激性气味的气体。写出 SOCl2 与水的化学方程式:____________。
)沸点为 77℃,遇水剧烈反应,产生酸雾和刺激性气味的气体。写出 SOCl2 与水的化学方程式:____________。
(5)同时满足下列条件的 C 的同分异构体共有______________种。写出其中一种结构简式______________。
a.在酸性条件下完全水解,得到两种产物:有机物 M 和碳酸(![]() )
)
b.M 分子中有 4 种不同化学环境的氢,且能与 FeCl3 溶液发生显色反应。
(6)已知:R'-CHO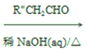 R'-CH=CCHO (R1、R2 代表烃基或 H),请结合上述信息,写出以
R'-CH=CCHO (R1、R2 代表烃基或 H),请结合上述信息,写出以![]() 和乙醛为主要原料制备
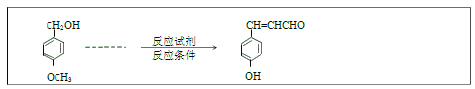
和乙醛为主要原料制备 ![]() 的合成路线流程图_____________(无机试剂任选):
的合成路线流程图_____________(无机试剂任选):
【答案】4-甲基苯酚或对甲基苯酚 14 醚键、羧基 取代反应 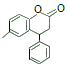 +2 NaOH
+2 NaOH![]()
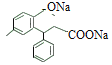 +H2O SOCl2+H2O=SO2+2HCl 2
+H2O SOCl2+H2O=SO2+2HCl 2 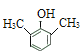 、
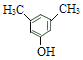
、
【解析】
(1)有机物命名,A(![]() )以苯酚为母体,苯环上的甲基与羟基对位关系,名称为4-甲基苯酚或对甲基苯酚;共面问题,苯环上的原子在同一个平面上,另外甲基上的C原子采用的sp3杂化,单键可以旋转,故甲基上的有一个氢原子可能在苯环所构成的这个平面上;
)以苯酚为母体,苯环上的甲基与羟基对位关系,名称为4-甲基苯酚或对甲基苯酚;共面问题,苯环上的原子在同一个平面上,另外甲基上的C原子采用的sp3杂化,单键可以旋转,故甲基上的有一个氢原子可能在苯环所构成的这个平面上;
(2)从反应物和生成物的结构简式上可以看出D中的Cl原子被![]() 所取代,故D→E的反应类型为取代反应;
所取代,故D→E的反应类型为取代反应;
(3)酯的水解反应,注意这个酯与其他的酯的不同之处,它水解生成的酚羟基也可以与氢氧化钠反应,故1molB 与 NaOH 溶液加热条件下反应,消耗2mol NaOH,反应方程式为 +2 NaOH
+2 NaOH![]()
 +H2O;
+H2O;
(4)结合题中的已知信息,推测生成物为SO2、HCl,然后写出相应的化学反应方程式;
(5)满足下列条件的 C 的同分异构体a.在酸性条件下完全水解,得到两种产物:有机物 M 和碳酸(![]() );b.M 分子中有 4 种不同化学环境的氢,且能与 FeCl3 溶液发生显色反应,M分子中含有酚羟基,满足条件的M的结构简式有:
);b.M 分子中有 4 种不同化学环境的氢,且能与 FeCl3 溶液发生显色反应,M分子中含有酚羟基,满足条件的M的结构简式有: 、
、 ,符合条件的C的同分异构体共2种;
,符合条件的C的同分异构体共2种;
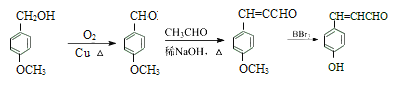
(6)结合已知提示信息和托特罗定一种合成路线流程图中的信息,进行新的流程图设计,![]() 与O2在Cu作催化剂的条件下催化氧化生成
与O2在Cu作催化剂的条件下催化氧化生成![]() ,结合题中所给已知信息,
,结合题中所给已知信息,![]() 与乙醛在稀的氢氧化钠溶液加热的条件下反应生成
与乙醛在稀的氢氧化钠溶液加热的条件下反应生成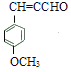 ,再结合流程图中的信息,
,再结合流程图中的信息, 在BBr3作用下生成
在BBr3作用下生成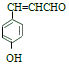 。
。
(1)A(![]() )以苯酚为母体,名称为4-
)以苯酚为母体,名称为4-
(2)D中的Cl原子被![]() 所取代,故D→E的反应类型为取代反应;
所取代,故D→E的反应类型为取代反应;
(3)B分子中含有酯基,在NaOH溶液中发生水解反应, +2 NaOH
+2 NaOH![]()
 +H2O;
+H2O;
(4)液态 SOCl2(![]() )沸点为 77℃,遇水剧烈反应,产生酸雾和刺激性气味的气体,该刺激性气味的气体为SO2,另一种物质是HCl,SOCl2 与水的化学方程式:SOCl2+H2O=SO2+2HCl;
)沸点为 77℃,遇水剧烈反应,产生酸雾和刺激性气味的气体,该刺激性气味的气体为SO2,另一种物质是HCl,SOCl2 与水的化学方程式:SOCl2+H2O=SO2+2HCl;
(5)同时满足下列条件的 C 的同分异构体a.在酸性条件下完全水解,得到两种产物:有机物 M 和碳酸(![]() );b.M 分子中有 4 种不同化学环境的氢,且能与 FeCl3 溶液发生显色反应,M分子中含有酚羟基,满足条件的M的结构简式有:
);b.M 分子中有 4 种不同化学环境的氢,且能与 FeCl3 溶液发生显色反应,M分子中含有酚羟基,满足条件的M的结构简式有: 、
、 ,符合条件的C的同分异构体共2种;
,符合条件的C的同分异构体共2种;
(6)![]() 与O2在Cu作催化剂的条件下催化氧化生成
与O2在Cu作催化剂的条件下催化氧化生成![]() ,结合题中所给已知信息,
,结合题中所给已知信息,![]() 与乙醛在稀的氢氧化钠溶液加热的条件下反应生成
与乙醛在稀的氢氧化钠溶液加热的条件下反应生成 ,再结合流程图中的信息,
,再结合流程图中的信息, 在BBr3作用下生成
在BBr3作用下生成 ,具体合成路线如下:
,具体合成路线如下: 。
。

【题目】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3H2O | 1.8×10-5 |
下表是常温下几种难(微)溶物的溶度积常数(Ksp):
难(微)溶物 | 溶度积常数(Ksp) |
BaSO4 | 1×10-10 |
BaCO3 | 2.6×10-9 |
CaSO4 | 7×10-5 |
CaCO3 | 5×10-9 |
请回答下列问题:
(l)写出HCN的电离方程式:___________,HClO的电子式__________。
(2)表中所给的四种酸中,酸性最强的是__________(用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大且电离常数改变的操作是__________(填字母序号)。
A.加少量冰酷酸 B.降低温度 C.加水稀释 D.升高温度 E.加少量的CH3COONa固体
(3)CH3COONH4的水溶液呈__________(选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是__________。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BasO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.02 mol·L-1,则溶液中CO32-物质的量浓度应≥__________mol·L-1。