题目内容
1.理论上存在的氟氯溴碘甲烷(CFClBrI)极难合成,下列有关CFClBrI的说法不正确的是( )| A. | 分子的立体结构为正四面体 | B. | 碳原子以sp3杂化 | ||
| C. | 属于极性分子 | D. | 有手性异构体 |
分析 A.C原子连接的四个原子不相同,CFClBrI为四面体构型,但不是正四面体;
B.C原子形成4个σ价,杂化轨道数目为4;
C.分子不是对称结构,正负电荷重心不重合;
D.氟氯溴碘甲烷中碳原子为手性碳原子,存在手性异构体.
解答 解:A.C原子连接的四个原子不相同,CFClBrI为四面体构型,但不是正四面体,故A错误;
B.C原子形成4个σ价,杂化轨道数目为4,碳原子以sp3杂化,故B正确;
C.分子不是对称结构,正负电荷重心不重合,氟氯溴碘甲烷属于极性分子,故C正确;
D.氟氯溴碘甲烷中碳原子为手性碳原子,存在手性异构体,故D正确,
故选A.
点评 本题考查分子构型判断、杂化方式、分子极性、手性异构,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列说法正确的是( )
| A. | 同一种元素各核素的质量数不同,但它们的化学性质几乎完全相同 | |
| B. | 任何元素的原子都是由核外电子和核内质子、中子组成 | |
| C. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H互称为核素 | |
| D. | ${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca、${\;}_{18}^{40}$Ar的质量数相同,所以它们是同位素 |
6.在1.01×105Pa下,1mol的下列物质的体积不同的是( )
| A. | 10℃时的HCl和H2O | B. | 400K时的水和CO2 | ||
| C. | 20℃时的氧气和空气 | D. | 常温下的H2和N2 |
5.下列说法不正确的是( )
| A. | 煤和石油都是混合物 | |
| B. | 石油通过催化重整可获得环状烃 | |
| C. | 煤的干馏和石油的分馏发生的都是化学变化 | |
| D. | 用溴的四氯化碳溶液可鉴别分馏获得的汽油和裂化获得的汽油 |
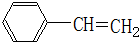 .
. .
.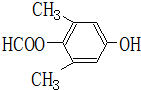 、
、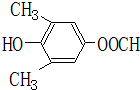 .
.