题目内容
(18分)甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计了如下实验流程:
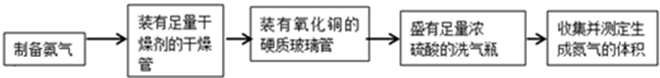
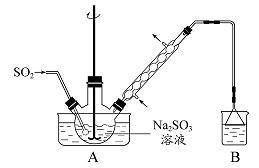
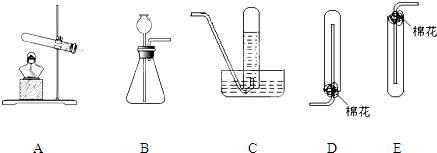
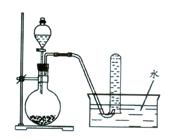
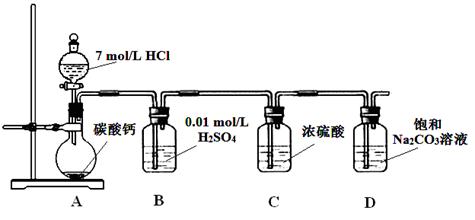
实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装 置,立即加热氧化铜。反应完成后,黑色氧化铜转化为红色的铜。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。

甲小组测得:反应前氧化铜的质量m1 g、氧化铜反应后剩余固体的质量m2g、生成氮气在标准状况下的体积V1L。乙小组测得:洗气前装置D的质量m3g、洗气后装置D的质量为m4g、生成氮气在标准状况下的体积V2L。请回答下列问题:
(1)检查A装置气密性的操作是____________________________________________________。
(2)实验室检验氨气的操作和现象是____________________________________。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备制备原理填写在下表的空格中。
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为________________。
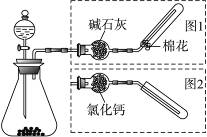
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数之比明显小于理论值,其原因是_______。为此,乙小组在原有实验的基础上增加了一个装有某药晶的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果。该药品的名称是________。

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装 置,立即加热氧化铜。反应完成后,黑色氧化铜转化为红色的铜。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。

甲小组测得:反应前氧化铜的质量m1 g、氧化铜反应后剩余固体的质量m2g、生成氮气在标准状况下的体积V1L。乙小组测得:洗气前装置D的质量m3g、洗气后装置D的质量为m4g、生成氮气在标准状况下的体积V2L。请回答下列问题:
(1)检查A装置气密性的操作是____________________________________________________。
(2)实验室检验氨气的操作和现象是____________________________________。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备制备原理填写在下表的空格中。
| | 实验装置 | 实验药品 | 制备原理 |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为____________ |
| 乙小组 | _____ | 浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用:_______ |
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数之比明显小于理论值,其原因是_______。为此,乙小组在原有实验的基础上增加了一个装有某药晶的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果。该药品的名称是________。
(1)连接导管,将导管插入水中,加热试管,导管口有气泡产生;停止加热,导管内有水回流并形成一段稳定的水柱
(2)用湿润的红色石蕊试纸接近导管口,试纸变蓝(或蘸有浓盐酸的玻璃棒接近导管口,产生白烟)
(3)(NH4)2SO4+Ca(OH)2△2NH3↑+2H2O+CaSO4;B;氢氧化钠溶于水后放热使氨气溶解度降低,增加OH-浓度,使NH3+H2O NH3·H2O
NH3·H2O OH-+NH4+向逆反应方向移动,加快氨气逸出。
OH-+NH4+向逆反应方向移动,加快氨气逸出。
(4)5V1:7(m1-m2)
(5)洗气瓶D中的浓硫酸不但吸收了反应生成的水,还吸收了未反应的氨气,从而使计算的氢的量偏高;碱石灰(或无水硫酸铜、氢氧化钠、氧化钙等)
(2)用湿润的红色石蕊试纸接近导管口,试纸变蓝(或蘸有浓盐酸的玻璃棒接近导管口,产生白烟)
(3)(NH4)2SO4+Ca(OH)2△2NH3↑+2H2O+CaSO4;B;氢氧化钠溶于水后放热使氨气溶解度降低,增加OH-浓度,使NH3+H2O
 NH3·H2O
NH3·H2O OH-+NH4+向逆反应方向移动,加快氨气逸出。
OH-+NH4+向逆反应方向移动,加快氨气逸出。(4)5V1:7(m1-m2)
(5)洗气瓶D中的浓硫酸不但吸收了反应生成的水,还吸收了未反应的氨气,从而使计算的氢的量偏高;碱石灰(或无水硫酸铜、氢氧化钠、氧化钙等)
试题分析:(1)检查A装置气密性一般是依据压强变化检验,具体操作方法是连接导管,将导管插入水中,用手紧握试管,导管口有气泡产生;松开手后,导管内有水回流并形成一段稳定的水柱。
(2)氨气是碱性气体,据此可以检验,即用湿润的红色石蕊试纸接近导管口,试纸变蓝(或蘸有浓盐酸的玻璃棒接近导管口,产生白烟)。
(3)①氢氧化钙与硫酸铵反应生成硫酸钙、氨气和水,反应的化学方程式为(NH4)2SO4+Ca(OH)2△2NH3↑+2H2O+CaSO4 。浓氨水是液体,氢氧化钠是固体,为使氨气逸出,采用加热降低氨气的溶解度,故选B装置。由于氢氧化钠固体溶于水后放热使氨气溶解度降低,同时增加溶液中OH-浓度,使NH3+H2O
 NH3·H2O
NH3·H2O OH-+NH4+向逆反应方向移动,从而加快氨气逸出。
OH-+NH4+向逆反应方向移动,从而加快氨气逸出。(4)反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g,则氧化铜中氧元素的质量为m1-m2,生成的水中氧元素的质量等于氧化铜氧元素的质量,则生成的水中氧原子的个数为
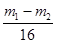 ,水中氢原子个数是氧原子个数的两倍,因此氢原子个数为
,水中氢原子个数是氧原子个数的两倍,因此氢原子个数为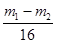 ×2,生成的氮气在标准状况下的体积V1L,则氮气中氮原子的个数为
×2,生成的氮气在标准状况下的体积V1L,则氮气中氮原子的个数为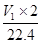 ,因此氮氢原子个数比为
,因此氮氢原子个数比为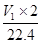 :
: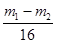 ×2=5V1:7(m1-m2);
×2=5V1:7(m1-m2);(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是洗气瓶D中的浓硫酸不但吸收了反应生成的水,还吸收了未反应的氨气,从而使计算的氢的量偏高. 因此在洗气瓶D前的位置应增加了一个装有碱石灰(氢氧化钠、氧化钙等)的实验仪器只吸收水,减小误差。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


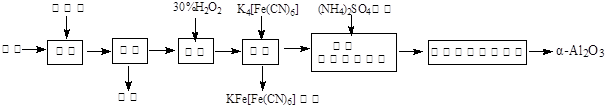
 2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过图9所示的装置。
2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过图9所示的装置。