题目内容
14.下列离子方程式正确的是( )| A. | 乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |
| B. | 澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O$\stackrel{△}{→}$2C6H5OH+CO32- | |
| D. | 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
分析 A.乙酸为弱酸,离子方程式中不能拆开;
B.碳酸氢钠过量,离子方程式按照氢氧化钙的化学式组成书写;
C.二氧化碳少量,苯酚的酸性大于碳酸氢根离子,二者反应生成苯酚和碳酸氢根离子;
D.甲醛分子中相当于含有2个醛基,能够与银氨溶液发生银镜反应.
解答 解:A.CH3COOH为弱酸,在离子方程式中应写成化学式,反应的离子方程式为:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO-,故A错误;
B.澄清石灰水中加入过量的碳酸氢钠溶液,反应生成碳酸钙沉淀、碳酸钠和水,正确的离子方程式为:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32-,故B错误;
C.苯酚钠溶液中通入少量二氧化碳,反应生成苯酚和碳酸氢根离子,正确的离子方程式为:C6H5O-+CO2+H2O$\stackrel{△}{→}$C6H5OH+HCO3-,故C错误;
D.甲醛溶液与足量的银氨溶液共热发生银镜反应,反应的离子方程式为:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
4.向含有0.078mo l的FeCl2溶液中通入0.009molCl2,再加入含0.01molX2O72-的酸性溶液,使溶液中的Fe2+恰好全部氧化,并使X2O72-还原为Xn+,则n的值是( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
5.下列化学用语表达正确的是( )
| A. | 一氯乙烷的结构式CH3Cl | B. | 丁烷的结构简式CH3(CH2)2CH3 | ||
| C. | 四氯化碳的电子式  | D. | 苯的分子式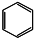 |
2.下列关于常见有机物的说法不正确的是 ( )
| A. | 食用植物油水解均可生成甘油 | |
| B. | 聚丙烯能使溴水褪色 | |
| C. | 苯和浓硝酸反应生成硝基苯,乙酸和乙醇反应生成乙酸乙酯,二者反应类型相同 | |
| D. | 向蔗糖水解后的溶液中加新制的Cu(OH)2悬浊液,加热到沸腾即可验证水解产物葡萄糖 |
9.下列有关氯气的叙述中,正确的是( )
| A. | 工业上常用MnO2和浓盐酸共热来制取氯气 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 在氧化还原反应中,Cl2只能作氧化剂 | |
| D. | 若提供含0.4 mol HCl的浓盐酸,MnO2过量,则可制得标准状况下氯气2.24 L |
19.关于溶液中微粒的浓度,下列说法正确的是( )
| A. | 0.1mol•L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 等浓度等体积的NaHSO3溶液与NaClO溶液混合后:c(Na++c(H+)═c(HSO3-)+c(ClO-)+2c(SO32-)+c(OH-) | |
| C. | 等浓度等体积的NaHCO3溶液与NaCl溶液混合后:$\frac{1}{2}$ c(Na+)═c(HCO3-)+c(CO32-)+c(H2CO3) | |
| D. | 标况下,将2.24LSO2气体通入到100ml 1mol•L-1的NaOH溶液中,完全反应后溶液呈酸性,则该溶液中: c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-) |
6.分子式为C5H9O2Cl,属于卤代酯且能发生银镜反应的同分异构体共有( )
| A. | 10种 | B. | 11种 | C. | 12种 | D. | 13种 |
3.中学化学中很多“规律”都可以类推,下列根据有关“规律”推出的结论正确的是( )
| A. | 硅是半导体材料,故同族的锗也是半导体材料 | |
| B. | 浓硫酸可以干燥HCl气体,故也可用浓硫酸干燥HI气体 | |
| C. | Na在空气中燃烧会生成Na2O2,故Li在空气中燃烧也会生成Li2O2 | |
| D. | 卤族元素单质随核电荷数增加熔点升高,故碱金属单质熔点也随核电荷数增加而升高 |