题目内容
2.下列关于常见有机物的说法不正确的是 ( )| A. | 食用植物油水解均可生成甘油 | |
| B. | 聚丙烯能使溴水褪色 | |
| C. | 苯和浓硝酸反应生成硝基苯,乙酸和乙醇反应生成乙酸乙酯,二者反应类型相同 | |
| D. | 向蔗糖水解后的溶液中加新制的Cu(OH)2悬浊液,加热到沸腾即可验证水解产物葡萄糖 |
分析 A、食用植物油为高级脂肪酸甘油酯;
B、聚丙烯中不存在碳碳双键;
C、苯与浓硝酸发生取代反应生成硝基苯;乙酸与乙醇发生酯化反应生成乙酸乙酯,酯化反应为取代反应;
D、葡萄糖中含有醛基,能与新制取Cu(OH)2悬浊液反应生成砖红色沉淀.
解答 解:A、食用植物油为高级脂肪酸甘油酯,水解得到甘油和高级脂肪酸,故A正确;
B、聚丙烯中不存在碳碳双键,不能使溴水褪色,故B错误;
C、苯与浓硝酸发生取代反应生成硝基苯;乙酸与乙醇发生酯化反应生成乙酸乙酯,酯化反应为取代反应,二者均为取代反应,故C正确;
D、葡萄糖中含有醛基,能与新制取Cu(OH)2悬浊液反应生成砖红色沉淀,故能利用此验证葡萄糖的存在,故D正确,
故选B.
点评 本题主要考查的是葡萄糖的验证、油脂的组成、常见有机化学反应类型判断,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列各组化合物的水溶液中,碱的碱性减弱,酸的酸性增强的是( )
| A. | NaOH,LiOH,HNO3,H3PO4 | B. | Mg(OH)2,Al(OH)3,HBrO4,HClO4 | ||
| C. | Mg(OH)2,Ca(OH)2,H3PO4,H2SO4 | D. | NaOH,Mg(OH)2,H3PO4,HClO4 |
17.如图为氢氧燃料电池原理示意图,下列叙述不正确的是( )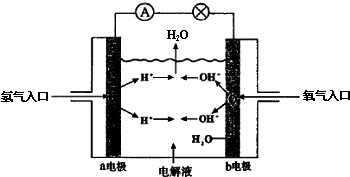

| A. | a电极是负极 | B. | b电极上发生氧化反应 | ||
| C. | 该电池工作时化学能转化为电能 | D. | 该电池的总反应为2H2+O2═2H2O |
7. 用纯净的CaCO3与100mL稀盐酸制取CO2实验过程记录如图(CO2的体积已折算成标准状态下的数值).下列分析错误的是( )
用纯净的CaCO3与100mL稀盐酸制取CO2实验过程记录如图(CO2的体积已折算成标准状态下的数值).下列分析错误的是( )
 用纯净的CaCO3与100mL稀盐酸制取CO2实验过程记录如图(CO2的体积已折算成标准状态下的数值).下列分析错误的是( )
用纯净的CaCO3与100mL稀盐酸制取CO2实验过程记录如图(CO2的体积已折算成标准状态下的数值).下列分析错误的是( )| A. | 第1到第2分钟间混合物质质量减少最快 | |
| B. | EF段中,用盐酸表示该反应的平均速率为0.4mol•L-1•min-1 | |
| C. | OE、EF、FG三段中用CO2表示该反应的平均速率之比为2:4:1 | |
| D. | FG段溶液质量增加比EF段溶液质量增加快 |
14.下列离子方程式正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |
| B. | 澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O$\stackrel{△}{→}$2C6H5OH+CO32- | |
| D. | 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
11.水杨酸环已酯具有花香气味,可作为香精配方.其合成路线如下:下列说法正确的是( )
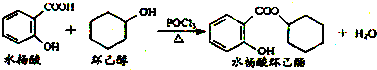
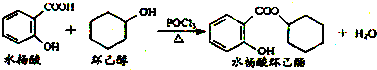
| A. | 水杨酸能分别与NaHCO3、Na2CO3溶液反应,且1 mol水杨酸分别消耗NaHCO32mol、Na2CO31mol | |
| B. | 水杨酸、环己醇和水杨酸环己酯均能与FeCl3溶液发生显色反应 | |
| C. | 1 mol水杨酸环己酯在NaOH溶液中水解时,最多消耗3 mol NaOH | |
| D. | 1 mol水杨酸跟足量浓溴水反应时,最多消耗Br2 2 mol |
12.把纯碘化氢气体装入密闭容器中,它将按2HI?H2+I2反应进行分解(正反应吸热),当系统在趋向平衡状态的过程中,以下描述正确的是( )
| A. | 碘化氢的生成速率大于其分解速率 | |
| B. | 碘化氢的生成速率等于其分解速率 | |
| C. | 加催化剂不会影响达到平衡的时间 | |
| D. | 升高温度可以缩短到达平衡状态的时间 |
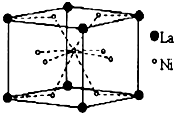 储氢材料的种类很多,包括储氢合金、配位氢化物、碳质吸附材料等.
储氢材料的种类很多,包括储氢合金、配位氢化物、碳质吸附材料等. 中相应官能团的名称及化学式
中相应官能团的名称及化学式