题目内容
3.相同物质的量的Na、Fe、Al分别跟足量的稀硫酸反应,生成的气体在同温同压下体积比为( )| A. | 1:2:3 | B. | 46:56:27 | C. | 6:3:2 | D. | 1/23:1/28:1/9 |
分析 相同物质的量的Na、Fe、Al分别与足量的稀硫酸反应,依据电子守恒计算生成氢气气体体积比.
解答 解:相同物质的量的镁、铝、铁分别与足量的稀硫酸反应,
2Na~2e-~H2
Fe~2e-~H2
Al~3e-~1.5H2
所以相同物质的量的Na、Fe、Al分别与足量的稀硫酸反应生成相同状况下氢气的体积比=物质的量之比=0.5:1:1.5=1:2:3;
故选A.
点评 本题考查了金属和酸反应的定量关系分析计算应用,应用电子守恒直接就是定量关系是较简洁的方法,题目较简单.

练习册系列答案
相关题目
13.如表除去括号内杂质所用的试剂和方法都正确的是( )
| 选项 | 物质 | 所用试剂 | 方法 |
| A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| B | 乙醇(水) | 生石灰 | 分液 |
| C | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
| D | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
11.在容积不变的密闭容器中存在如下反应:2A(g)+B(g)?3C(g);△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )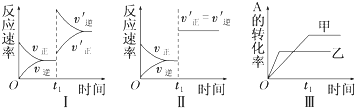

| A. | 图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响 | |
| B. | 图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响 | |
| C. | 图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高 | |
| D. | 图Ⅲ表示的是不同催化剂对平衡的影响,且甲的催化效率比乙高 |
18.下列物质中能使干燥的红色石蕊试纸变蓝色的是( )
| A. | 氨气 | B. | 氨水 | C. | 液氨 | D. | 氯化铵 |
8.下列关于化学反应限度的说法中不正确的是( )
| A. | 当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度 | |
| B. | 当一个可逆反应达到平衡状态时,各组分浓度不变,v(正)=v(逆)=0 | |
| C. | 任何可逆反应的进程都有一定的限度,只是不同的反应限度不同 | |
| D. | 化学反应的限度可以通过改变条件而改变 |
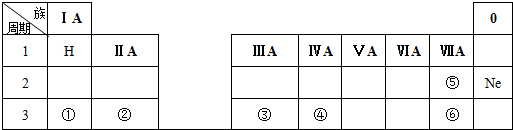
15.下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne,可用于制半导体材料的元素是Si.
(2)B的最高价氧化物对应的水化物与C的单质反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
(3)最高价氧化物对应的水化物中酸性最强的是HClO4;
(4)A分别与D、E、G、H形成的化合物中,最稳定的是HF;
(5)在B、C、D中,原子半径由大到小的顺序是Na>Al>C.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)B的最高价氧化物对应的水化物与C的单质反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
(3)最高价氧化物对应的水化物中酸性最强的是HClO4;
(4)A分别与D、E、G、H形成的化合物中,最稳定的是HF;
(5)在B、C、D中,原子半径由大到小的顺序是Na>Al>C.
12.化学无处不在,下列与化学有关的说法正确的是( )
| A. | 日常生活中无水乙醇常用于杀菌消毒 | |
| B. | 棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O | |
| C. | 加热能杀死流感病毒式因为病毒的蛋白质受热变性 | |
| D. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
17.医学界通过用放射性14C标记的C60,发现C60的羧酸衍生物在特定条件下可断裂DNA杀死细胞,抑制艾滋病.关于14C的下列说法中正确的是( )
| A. | 14C原子与C60中普通碳原子的化学性质相同 | |
| B. | 14C原子与14N原子所含中子数相同 | |
| C. | 14C是C60的同素异形体 | |
| D. | 14CO与12CO、13CO是碳元素的三种同位素 |