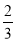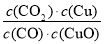题目内容
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是( )
①w=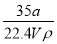 ×100%
×100%
②c=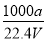
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w
④若上述溶液中再加入0.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为c(NH4+)>c(Cl-)>c(OH-)>c(H+)
A.①④ B.②③ C.①③ D.②④
D
【解析】①w= ×100%=
×100%=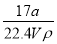 ×100%;②c=
×100%;②c=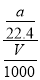 =
=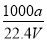 ;③因为V mL水的质量大于V mL氨水的质量,所以溶液的质量分数小于0.5w;④所得溶液为NH4Cl和NH3·H2O等物质的量的混合液,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+)。
;③因为V mL水的质量大于V mL氨水的质量,所以溶液的质量分数小于0.5w;④所得溶液为NH4Cl和NH3·H2O等物质的量的混合液,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+)。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案A、B、D、E四种元素均为短周期元素,原子序数逐渐增大。A元素原子的核外电子数、电子层数和最外层电子数均相等。B、D、E三种元素在周期表中的相对位置如图①所示,只有E元素的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、B两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质;X分子含有10个电子。它们之间的转化关系如图②所示。
B | D |
|
|
| E |
图①
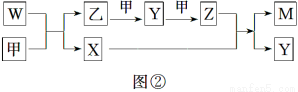
请回答下列问题:
(1)Z的化学式为__________________。
(2)E的单质与水反应的离子方程式为________________________________________。
(3)W?空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。W?空气燃料电池放电时,正极反应式为________________________________,负极反应式为____________________。
(4)将一定量的A2、B2的混合气体放入1 L密闭容器中,在500 ℃、2×107 Pa下达到平衡。测得平衡气体的总物质的量为0.50 mol,其中A2为0.3 mol,B2为0.1 mol。则该条件下A2的平衡转化率为________,该温度下的平衡常数为____________(结果保留3位有效数字)。