题目内容
19.下列各组离子在酸性溶液中能大量共存的是( )| A. | Fe3+、NH4+、SCN-、C1- | B. | Na+、Br-、NH4+、SO42- | ||
| C. | Na+、HCO3-、K+、CO32- | D. | Fe2+、NH4+、C1-、OH- |
分析 A.铁离子与硫氰根离子结合生成硫氰化铁;
B.四种离子之间不反应,都不与酸性溶液中的氢离子反应;
C.碳酸氢根离子、碳酸根离子都与酸性溶液反应;
D.亚铁离子与氢氧根离子反应生成氢氧化亚铁,氢氧根离子与酸性溶液反应.
解答 解:A.Fe3+、SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,故A错误;
B.Na+、Br-、NH4+、SO42-之间不发生反应,都不与酸性溶液反应,在溶液中能够大量共存,故B正确;
C.HCO3-、CO32-都与酸性溶液反应,在溶液中不能大量共存,故C错误;
D.Fe2+与OH-反应生成氢氧化亚铁,OH-与酸性溶液反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
9.下列气体在水中溶解度最大的是( )
| A. | NO | B. | SO2 | C. | CO2 | D. | Cl2 |
7.下列各组物质,在常温下不发生反应的是( )
①硫化氢和二氧化硫 ②铝与氧化铁 ③铜与稀硝酸 ④石英与纯碱
⑤一氧化氮与氧气 ⑥硅与氧气.
①硫化氢和二氧化硫 ②铝与氧化铁 ③铜与稀硝酸 ④石英与纯碱
⑤一氧化氮与氧气 ⑥硅与氧气.
| A. | ②③⑤ | B. | ②④⑥ | C. | ①②⑥ | D. | ①③⑤ |
14.根据下列各反应现象所归纳的元素性质不正确的是( )
| A. | 将一小块钠投入到盛有硫酸铜溶液的烧杯中,发现没有紫红色的铜析出.不能说明钠的金属性比铜弱 | |
| B. | 用湿润的淀粉碘化钾试纸放置在有氯气产生的导管上端,发现试纸变蓝.说明氯元素的非金属性比碘元素强 | |
| C. | 把H2S气体和Cl2在集气瓶中混合,一段时间后发现瓶壁有淡黄色固体析出.说明Cl的非金属性比S强 | |
| D. | 将0.1 mol Na、Mg、Al分别与足量稀盐酸反应,除共同产生H2外,还分别生成了NaCl、MgCl2、AlCl3,金属失去的电子数分别为0.1 mol、0.2 mol、0.3 mol.说明这三种金属的活泼性为:Al>Mg>Na |
4.金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式为:2CuFeS2+O2═□+2FeS+SO2,下列说法不正确的是( )
| A. | 方框中的物质应为 Cu2S | |
| B. | 若有1 molSO2生成,则反应中有4 mol 电子转移 | |
| C. | SO2既是氧化产物又是还原产物 | |
| D. | O2只作氧化剂 |
11.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
| A. | NaOH(s) | B. | CH3COONa(s) | C. | FeCl3(s) | D. | NH4Cl |
10.下列关于有机物的说法正确的是( )
| A. | 纯净物C4H8的核磁共振氢谱峰最多为4 | |
| B. | 化学式为C8H8的有机物,一定能使酸性高锰酸钾溶液褪色 | |
| C. | 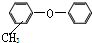 的同分异构体中,可以有醇、酚类物质 的同分异构体中,可以有醇、酚类物质 | |
| D. | 1 mol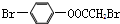 最多能与2 mol NaOH反应 最多能与2 mol NaOH反应 |