题目内容
1. 水是生命的源泉、工业的血液、城市的命脉.请回答下列问题:
水是生命的源泉、工业的血液、城市的命脉.请回答下列问题:(1)纯水在25℃时,pH=7,该温度下1mol•L-1的NaOH溶液中,由水电离出的
c(OH-)=10-14mol•L-1.
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为C${O}_{3}^{2-}$+H2O?HC${O}_{3}^{-}$+OH-、HC${O}_{3}^{-}$+H2OH2CO3+OH-,由水电离出的c(OH-)=0.001mol•L-1.
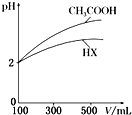
(3)体积均为100mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离常数小于(填“大于”“小于”或“等于”)CH3COOH的电离常数.理由是稀释相同倍数,一元酸HX的pH变化量比CH3COOH的小,故酸性较弱,电离常数较小.
(4)电离常数是衡量弱电解质电离程度强弱的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
分析 (1)NaOH是一元强碱,1mol/L的NaOH溶液中c(OH-)=1mol/L,据纯水在25℃时,pH=7可知,KW=10-14求算由水电离出来的c(OH-);
(2)碳酸钠溶液中因碳酸根离子水解导致溶液显碱性,盐溶液中盐的水解促进水的电离;
(3)据图分析,加水稀释的过程中,HX的pH变化比较慢,说明HX的酸性比醋酸弱;
(4))根据酸的电离常数进行分析判断,电离常数越大,对应盐的水解程度越小,溶液的pH越小.
解答 解:(1)1mol/L的NaOH溶液中c(OH-)=1mol/L,KW=10-14可知由水电离出来的c(OH-)=10-14mol/L,故答案为:10-14;
(2)碳酸钠溶液中因碳酸根离子水解导致溶液显碱性,碳酸根水解的离子方程式为C${O}_{3}^{2-}$+H2O?HC${O}_{3}^{-}$+OH-、HC${O}_{3}^{-}$+H2OH2CO3+OH-,其pH=11,则c(OH-)=0.001mol/L,全部由水电离产生,故答案为:C${O}_{3}^{2-}$+H2O?HC${O}_{3}^{-}$+OH-、HC${O}_{3}^{-}$+H2OH2CO3+OH-;0.001;
(3)据图分析,加水稀释的过程中,HX的pH变化比较慢,说明HX的酸性比醋酸弱,HX的电离平衡常数比醋酸小,
故答案为:小于;稀释相同倍数,一元酸HX的pH变化量比CH3COOH的小,故酸性较弱,电离常数较小;
(4)根据图表数据分析,电离常数:醋酸>HCN>碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,故溶液的pH为:Na2CO3溶液>NaCN溶液>CH3COONa溶液;故答案为:Na2CO3溶液>NaCN溶液>CH3COONa溶液.
点评 本题考查弱电解质的电离,根据平衡常数确定酸性强弱,从而确定水解程度,注意加水稀释时从各微粒的物质的量变化分析,难度中等.

| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 加CCl4,振荡、静置 | 上层溶液显紫色 | 原溶液中有I2 |
| C | 滴加NaOH溶液,将湿润 红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| D | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+ |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
| A. | FeCl2 | B. | Al2S3 | C. | CuCl2 | D. | Mg3N2 |
| A. | 通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 | |
| B. | 光线透过胶体时,胶体发生了丁达尔现象 | |
| C. | 用渗析的方法净化胶体时,半透膜只允许较小的分子、离子通过 | |
| D. | 胶体粒子具有较大的表面积,能吸附阳离子或阴离子,故在电场的作用下会产生电泳现象 |
| A. | 12C与14C互为同素异形体 | |
| B. | 14C的原子中有6个质子,8个电子 | |
| C. | 12C与14C的原子中含有的中子数之比为3:4 | |
| D. | 金刚石与C60都属于原子晶体 |
| A. | 由H原子形成1molH-H键要吸收热量 | |
| B. | C(石墨,s)═C(金刚石,s)△H=+1.9 kJ/mol,则可判定金刚石比石墨稳定 | |
| C. | 500℃、30 MPa下,0.5 mol N2(g)和1.5 mol H2(g)反应生成NH3(g)放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 已知Ni(CO)4(s)=Ni(s)+4CO(g)△H=Q kJ•mol-1,则Ni(s)+4CO(g)=Ni(CO)4(s)△H=-Q kJ•mol-1 |