题目内容
13.医学上通过放射性14C标记的C60进行跟踪研究,发现一种C60的羧酸衍生物在特定的条件下可通过断裂DNA杀死细胞,从而抑制艾滋病.有关C60和14C的叙述正确的是( )| A. | 12C与14C互为同素异形体 | |
| B. | 14C的原子中有6个质子,8个电子 | |
| C. | 12C与14C的原子中含有的中子数之比为3:4 | |
| D. | 金刚石与C60都属于原子晶体 |
分析 A.由同种元素形成的不同种单质互为同素异形体;
B.原子的质子数=电子数;
C.中子数=质量数-质子数;
D.相邻原子之间通过强烈的共价键结合而成的空间网状结构的晶体叫做原子晶体.
解答 解:A.12C与14C是原子,不是单质,不为同素异形体,故A错误;
B.14C的原子中有6个电子,故B错误;
C.中子数=质量数-质子数,12C与14C的原子中含有的中子数分别为6、8,中子数之比为3:4,故C正确;
D.C60 之间的相互作用力是范德华力,属于分子晶体,故D错误.
故选C.
点评 本题考查同素异形体、原子构成、晶体类型等,题目难度不大,注意原子符号左上角的数字为质量数.

练习册系列答案
相关题目
4.设NA为阿伏加德岁常数的值,下列叙述正确的是( )
| A. | 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 常温常压下,7.0g乙烯与丙烯的混合物中含有碳氢键的数目为NA | |
| C. | 50 mL18.4mol/L浓硫酸与足量铜微热反应,生成S02分子的数目为0.46NA | |
| D. | 某密闭容器盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0 6NA |
1. 水是生命的源泉、工业的血液、城市的命脉.请回答下列问题:
水是生命的源泉、工业的血液、城市的命脉.请回答下列问题:
(1)纯水在25℃时,pH=7,该温度下1mol•L-1的NaOH溶液中,由水电离出的
c(OH-)=10-14mol•L-1.
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为C${O}_{3}^{2-}$+H2O?HC${O}_{3}^{-}$+OH-、HC${O}_{3}^{-}$+H2OH2CO3+OH-,由水电离出的c(OH-)=0.001mol•L-1.
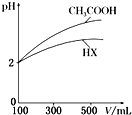
(3)体积均为100mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离常数小于(填“大于”“小于”或“等于”)CH3COOH的电离常数.理由是稀释相同倍数,一元酸HX的pH变化量比CH3COOH的小,故酸性较弱,电离常数较小.
(4)电离常数是衡量弱电解质电离程度强弱的物理量.已知:
25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液.
 水是生命的源泉、工业的血液、城市的命脉.请回答下列问题:
水是生命的源泉、工业的血液、城市的命脉.请回答下列问题:(1)纯水在25℃时,pH=7,该温度下1mol•L-1的NaOH溶液中,由水电离出的
c(OH-)=10-14mol•L-1.
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为C${O}_{3}^{2-}$+H2O?HC${O}_{3}^{-}$+OH-、HC${O}_{3}^{-}$+H2OH2CO3+OH-,由水电离出的c(OH-)=0.001mol•L-1.
(3)体积均为100mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离常数小于(填“大于”“小于”或“等于”)CH3COOH的电离常数.理由是稀释相同倍数,一元酸HX的pH变化量比CH3COOH的小,故酸性较弱,电离常数较小.
(4)电离常数是衡量弱电解质电离程度强弱的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
8.下列离子方程式书写正确的是( )
| A. | 石灰乳与Na2CO3溶液混合:Ca2++C${O}_{3}^{2-}$═CaCO3↓ | |
| B. | NH4HSO3溶液与足量NaOH溶液混合加热: N${H}_{4}^{+}$+HS${O}_{3}^{-}$+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+S${O}_{3}^{2-}$+2H2O | |
| C. | 氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++S${O}_{4}^{2-}$+H++OH-═BaSO4↓+H2O |
18.在有催化剂存在的条件下,将2体积的SO2和1体积的O2混合装入密闭容器中并加热一段时间后,将混合气体通入BaCl2溶液中,产生的沉淀( )
| A. | 不可能是BaSO4 | B. | 一定是BaSO3 | ||
| C. | 一定是BaSO4 | D. | 一定是BaSO3和BaSO4 |
2.下列说法正确的是( )
| A. | 电解饱和食盐水可制得金属钠 | |
| B. | 通过化学反应从海水中可提取氯化钠、溴、碘等物质 | |
| C. | 为了增强高锰酸钾溶液的氧化性可用盐酸酸化 | |
| D. | ClO2是一种有刺激性气味的黄绿色气体,除用于杀菌消毒外,还广泛用于环保、漂白、除臭 等方面 |
3.下列离子方程式正确的是( )
| A. | 碳酸钙和盐酸反应:CaCO3+2H+═H2O+CO2↑+Ca2+ | |
| B. | 铜片插入硝酸银溶液:Cu+Ag+═Cu2++Ag | |
| C. | 溴水滴入碘化钾溶液:Br2+I-═Br-+I2 | |
| D. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
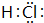 .
.