题目内容
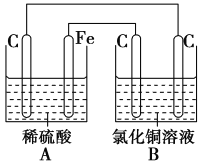
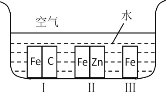
【题目】(1)如图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_______________。
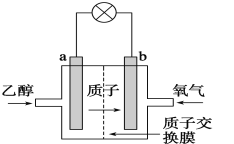
(2)氟氯代烷是一种能破坏臭氧层的物质。在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:①Cl+O3→ClO+O2 ②O3→O+O2 ③ClO+O→Cl+O2。上列的反应的总反应式是_________,少量氟氯代烷能破坏大量臭氧的原因是______________。
【答案】Ⅰ、Ⅲ、Ⅱ 2O3→3O2 氟氯代烷分解产生的Cl对O3的分解有促进作用
【解析】
(1)金属腐蚀的速度:原电池的负极金属>金属的化学腐蚀>有保护措施的腐蚀;
(2)将方程式①②③相加得出氧气和臭氧的关系式;根据Cl+O3→ClO+O2判断氟氯代烷能破坏大量臭氧的原因。
(1)铁处于Ⅰ的环境中做原电池的负极,腐蚀速率较快,铁处于Ⅱ的环境中做原电池的正极,被保护,腐蚀速率很慢,铁处于Ⅲ的环境中的金属铁发生化学腐蚀,速度较慢;故答案为:Ⅰ、Ⅲ、Ⅱ;
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2;氟氯代烷受紫外线的照射分解出氯原子,Cl+O3→ClO+O2,Cl对O3的分解有促进作用,所以能破坏臭氧层;故答案为:2O3→3O2;氟氯代烷分解产生的Cl对O3的分解有促进作用。

练习册系列答案
相关题目