题目内容
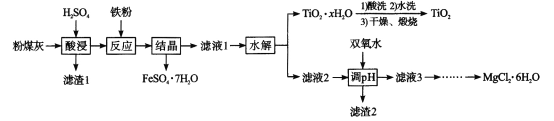
【题目】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:Ksp[ Al(OH)3]=1.0×10-34 Ksp[Fe(OH)3]=4.0×10 -38。已知::“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO42-和一种阳离子,该离子会水解,下列说法不正确的是
A.“酸浸”时TiO2发生反应的离子方程式为TiO2 +2H+= =TiO2+ +H2O
B.“结晶”时温度需控制在70℃以上,温度过低TiO2![]() xH2O产率降低
xH2O产率降低
C.为使滤渣2沉淀完全,需“调pH"最小为4.3
D.MgCl2溶液制备MgCl2![]() 6H2O需要在HCl的气氛下蒸发浓缩
6H2O需要在HCl的气氛下蒸发浓缩
【答案】B
【解析】
粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等,加入硫酸酸浸过滤得到滤渣1和滤液,氧化铝溶解生成硫酸铝,氧化亚铁溶解生成硫酸亚铁,氧化铁溶解生成硫酸铁,氧化镁溶解生成硫酸镁,“酸浸”后钛主要以TiOSO4形式存在,滤渣为二氧化硅,加入铁粉还原铁离子生成亚铁离子,结晶析出硫酸亚铁晶体,过滤,得到滤液1含硫酸铝、硫酸镁、TiOSO4、少量硫酸亚铁,水解过滤,TiOSO4生成TiO2xH2O,经酸洗水洗干燥和灼烧后得到TiO2,滤液2中含硫酸铝和硫酸镁、少量硫酸亚铁,加入过氧化氢氧化亚铁离子为铁离子,调节溶液pH使铝离子和铁离子全部沉淀,过滤得到滤渣2为氢氧化铁和氢氧化铝沉淀,滤液3含硫酸镁,最终获取MgCl2·6H2O。
A. 根据题干信息知“酸浸”后TiO2反应生成TiOSO4,TiOSO4电离产发生SO42-和TiO2+,则反应的离子方程式为TiO2 +2H+= =TiO2++H2O,故A正确;
B. “结晶”需控制在70℃左右,温度过高会导致TiO2+提前水解混入硫酸亚铁晶体,降低TiO2xH2O的产量,故B错误;
C. 调节溶液pH目的是铝离子、铁离子沉淀完全除去,因Ksp[ Al(OH)3]=1.0×10-34 ,Ksp[Fe(OH)3]=4.0×10-38,阴阳离子比相同,Ksp[ Al(OH)3] >Ksp[Fe(OH)3],则铝离子沉淀完全对应溶液pH最小,结合溶度积常数计算,c3(OH-)=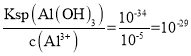 ,c(OH-)=10-9.6mol/L,c(H+)=
,c(OH-)=10-9.6mol/L,c(H+)=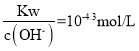 ,pH=4.3,故C正确;
,pH=4.3,故C正确;
D. 用MgCl2溶液制备MgCl26H2O,需要蒸发浓缩、冷却结晶、过滤洗涤、干燥等;因为加热蒸发促进氯化镁水解,为抑制氯化镁水解应在HCl的气氛下蒸发浓缩,故D正确;
故选B。

【题目】“绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对工业生产、缓解环境污染、解决能源危机等具有重要意义。
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-1651.0kJ/mol
CO还原氧化铁的热化学方程式为_____________。
(2)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
H2CO3 | H2S | |
Ka1 | 4.410-7 | 1.310-7 |
Ka2 | 4.710-11 | 7.110-15 |
①煤的气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为_______;
②常温下,0.1mol·L-1 NaHCO3溶液和0.1mol·L-1 NaHS溶液的pH相比,pH较小的为________ 溶液(填化学式)。
(3)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH (此反应在低温时为自发反应)。
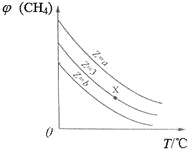
①下图能表示该反应的平衡常数K与温度T之间的变化关系曲线为_____(填“a”或“b”),其判断依据是__________。
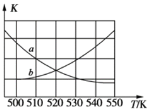
②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如下图所示,则在该时间段内,恰好达到化学平衡时,此时容器内的压强与反应开始时的压强之比为_____________。
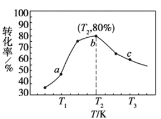
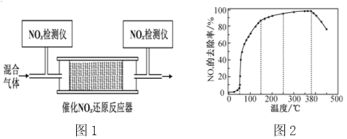
(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成28g N2时,转移的电子数为____mol(结果保留三位有效数字)。
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置如图1)。反应相同时间NOx的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是______;当反应温度高于380 ℃时,NOx的去除率迅速下降的原因可能是____。