题目内容
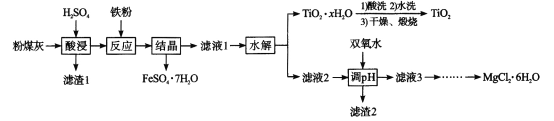
【题目】单质钛(Ti)抗腐蚀能力强(放在大海中几周后仍金光闪闪),机械强度高,有“未来金属”之称。又因用它制的“骨头”置入人体后可以在上面长肉,所以又有“亲生物金属”之美誉。工业上常用硫酸分解钛铁矿(FeTiO3,铁为+2价)的方法来制取TiO2,再由TiO2制金属钛。主要反应有:
①FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4
③H2TiO3![]() TiO2+H2O
TiO2+H2O
④TiO2+2C+2Cl2![]() TiCl4↑+2CO↑
TiCl4↑+2CO↑
⑤TiCl4+2Mg![]() 2MgCl2+Ti
2MgCl2+Ti
上述反应中,属于氧化还原反应的有( )
A.①②
B.①⑤
C.③④
D.④⑤
【答案】D
【解析】
有元素化合价变化的反应是氧化还原反应。
①FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O反应中,元素化合价都没变,属于非氧化还原反应;
②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4反应中,元素化合价都没变,属于非氧化还原反应;
③H2TiO3![]() TiO2+H2O反应中,元素化合价都没变,属于非氧化还原反应;
TiO2+H2O反应中,元素化合价都没变,属于非氧化还原反应;
④TiO2+2C+2Cl2![]() TiCl4↑+2CO↑反应中,碳元素化合价升高、氯元素化合价降低,有元素化合价变化,属于氧化还原反应;
TiCl4↑+2CO↑反应中,碳元素化合价升高、氯元素化合价降低,有元素化合价变化,属于氧化还原反应;
⑤TiCl4+2Mg![]() 2MgCl2+Ti反应中,镁元素化合价升高、钛元素化合价降低,有元素化合价变化,属于氧化还原反应;
2MgCl2+Ti反应中,镁元素化合价升高、钛元素化合价降低,有元素化合价变化,属于氧化还原反应;
综上所述,④⑤属于氧化还原反应,故选D。

 阅读快车系列答案
阅读快车系列答案【题目】甲醇是一种新型的汽车动力燃料。回答下列问题:
⑴工业上可通过![]() 和
和![]() 化合来制备甲醇。已知某些化学键的键能数据如下表:
化合来制备甲醇。已知某些化学键的键能数据如下表:
化学键 |
|
|
|
|
|
键能 | 413 | 436 | 358 | 1072 | 463 |
已知![]() 中的
中的![]() 与
与![]() 之间为三键,则工业制备甲醇的热化学方程式为________。
之间为三键,则工业制备甲醇的热化学方程式为________。
⑵某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为![]() 的密闭容器内充入
的密闭容器内充入![]() 和
和![]() ,加入合适催化剂(体积可以忽略不计),在
,加入合适催化剂(体积可以忽略不计),在![]() 时开始反应,并用压力计监测容器内压强的变化如下表:
时开始反应,并用压力计监测容器内压强的变化如下表:
反应时间/ | 0 | 5 | 10 | 15 | 20 | 25 |
压强/ | 10.8 | 9.6 | 8.4 | 7.8 | 7.2 | 7.2 |
则从反应开始到![]() 时,以
时,以![]() 表示的平均反应速率
表示的平均反应速率![]() ________,该温度下平衡常数
________,该温度下平衡常数![]() ________
________![]() ,若升高温度,则
,若升高温度,则![]() 值________(填“增大”“减小”或“不变")。
值________(填“增大”“减小”或“不变")。
⑶模拟工业合成甲醇的反应,下图是4种投料比![]() 分别为
分别为![]() 、
、![]() 、
、![]() 、
、![]() 下,反应温度对
下,反应温度对![]() 平衡转化率影响的曲线。
平衡转化率影响的曲线。

①曲线![]() 对应的投料比为________。
对应的投料比为________。
②当曲线![]() 、
、![]() 、
、![]() 对应的投料比达到相同的
对应的投料比达到相同的![]() 平衡转化率时,对应的反应温度与投料比的关系是________。
平衡转化率时,对应的反应温度与投料比的关系是________。
③投料比为![]() 、反应温度为
、反应温度为![]() 时,平衡混合气中
时,平衡混合气中![]() 的物质的量分数是________(精确到
的物质的量分数是________(精确到![]() )。
)。