题目内容
16.请填入相应化学试剂以除去括号中的杂质,并写出相应的化学反应方程式.(加入的试剂为适量,反应条件自行选择)(1)Na2SO4溶液(MgSO4)试剂:氢氧化钠溶液化学方程式:2NaOH+MgSO4═Na2SO4+Mg(OH)2↓
(2)Cu(CuO)试剂:稀硫酸化学方程式:H2SO4+CuO=CuSO4+H2O
(3)CO(CO2)试剂:氢氧化钠溶液化学方程式:CO2+2NaOH=Na2CO3+H2O.
分析 (1)除去硫酸钠中的硫酸镁,可以加入适量的氢氧化钠溶液,将硫酸镁反应生成氢氧化镁和硫酸钠;
(2)氧化铜能与稀盐酸反应生成氯化铜和水,铜不与稀盐酸反应,能除去杂质且没有引入新的杂质,符合除杂原则;
(3)CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,再通过浓硫酸除去水蒸气,能除去杂质且没有引入新的杂质,符合除杂原则.
解答 解:(1)Na2SO4溶液(MgSO4):向混合液中加入适量氢氧化钠溶液,将杂质硫酸镁转化成硫酸钠,反应的方程式为:2NaOH+MgSO4═Na2SO4+Mg(OH)2↓,
故答案为:氢氧化钠溶液;2NaOH+MgSO4═Na2SO4+Mg(OH)2↓;
(2)氧化铜能与过量的稀硫酸反应,铜不与稀硫酸反应,再进行过滤,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:H2SO4+CuO=CuSO4+H2O,
故答案为:稀硫酸;H2SO4+CuO=CuSO4+H2O;
(3)二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,一氧化碳不能与氢氧化钠溶液反应,反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O.
故答案为:氢氧化钠溶液;CO2+2NaOH=Na2CO3+H2O.
点评 本题考查了物质的分离与除杂、离子方程式的书写,题目难度中等,根据杂质、被提纯物质的性质正确选用除杂试剂为解答关键,明确选用的操作试剂在反应中不能引进引进新的杂质,其操作简单,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.室温下,对pH相等、体积相同的盐酸和醋酸分别进行以下操作,下列说法正确的是( )
| A. | 将温度迅速升高20℃,两溶液的pH均增大 | |
| B. | 加水稀释相同倍数后,两溶液的pH同等程度减小 | |
| C. | 加少量的醋酸钠固体后,两溶液的pH均增大 | |
| D. | 加足量的锌充分反应后,两溶液产生的氢气的量一样多 |
4.已知分解1mol H2O2放出热量98kJ,在含少量I-的溶液中,H2O2分解的机理为
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
| A. | I-是该反应的催化剂 | B. | IO-也是该反应的催化剂 | ||
| C. | 反应活化能等于98 kJ•mol-1 | D. | v(H2O2)=v(H2O)=v(O2) |
1.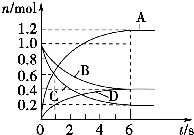 一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
 一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )| A. | 该反应的化学方程式为3B+4C?6A+2D | |
| B. | 反应进行到1 s时,v(A)和v(D)不相等 | |
| C. | 反应进行到6 s时,B的平均反应速率为0.05 mol•L-1•s-1 | |
| D. | 反应进行到6 s时,各物质的浓度不再变化,反应速率为零 |
5.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
(2)该反应为吸热反应(选填吸热、放热).
(3)能判断该反应是否达到化学平衡状态的依据是bc(多选不得分).
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)某温度下SO2的转化反应的2SO2(g)+O2(g)?2SO3(g)平衡常数K=532.4.
下面三个混合体系中各物质的浓度如下表:
试判断各体系中反应进行的方向:
体系(1)逆向体系(2)正向体系(3)已平衡(填正向、逆向或已平衡).
其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
(2)该反应为吸热反应(选填吸热、放热).
(3)能判断该反应是否达到化学平衡状态的依据是bc(多选不得分).
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)某温度下SO2的转化反应的2SO2(g)+O2(g)?2SO3(g)平衡常数K=532.4.
下面三个混合体系中各物质的浓度如下表:
| 体系 | c(SO2) mol/L | c(O2) mol/L | c(SO3) mol/L | 浓度商 |
| (1) | 0.0600 | 0.400 | 2.000 | 不填 |
| (2) | 0.0960 | 0.300 | 0.500 | 不填 |
| (3) | 0.0862 | 0.263 | 1.020 | 不填 |
体系(1)逆向体系(2)正向体系(3)已平衡(填正向、逆向或已平衡).
 1,2,3,4-四氢化萘的结构简式是
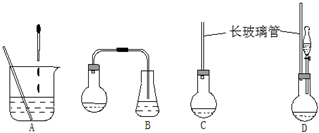
1,2,3,4-四氢化萘的结构简式是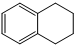 ,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2?C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水.有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2?C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水.有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下: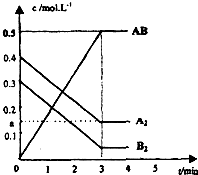 在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+B2(g)?2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示.
在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+B2(g)?2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示.